微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某温度时,在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如图所示,有关粒子浓度关系的比较正确的是
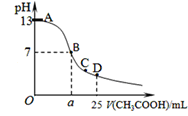
A.在D点:c(CH3COO-)+c(CH3COOH)=2c(Na+)
B.在C点:c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
C.在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
D.在A、B间任一点,溶液中一定都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
参考答案:A
本题解析:
试题分析:A项是物料守恒,对;B项、C点溶液显酸性,c(H+)>c(OH-),错;C项、在B点溶液显中性c(Na+)=c(CH3COO-)>c(OH-)=c(H+),错;在A、B间任一点,不一定有c(CH3COO-)>c(OH-),反应开始时c(OH-)比较大,错,选A。
考点:酸碱中和过程中溶液中的离子浓度比较。
本题难度:一般
2、选择题 下列溶液一定显酸性的是
A.含H+的溶液
B.c(OH-)<c(H+)的溶液
C.pH<7的溶液
D.能与金属Al反应放出H2的溶液
参考答案:B
本题解析:
试题分析:A.在任何物质的稀溶液中都含H+的溶液,所以,含有H+的溶液不一定显酸性。错误。B.在任何物质的稀溶液中都存在水的电离平衡:H2O H++OH-,当c(OH-)= c(H+)时溶液显中性;当c(OH-)<c(H+)时,溶液显酸性。当c(OH-)> c(H+)时溶液显碱性。正确。C.在任何物质的稀溶液中都存在水的电离平衡:H2O
H++OH-,当c(OH-)= c(H+)时溶液显中性;当c(OH-)<c(H+)时,溶液显酸性。当c(OH-)> c(H+)时溶液显碱性。正确。C.在任何物质的稀溶液中都存在水的电离平衡:H2O H++OH-。在室温下在纯水中,c(OH-)・c(H+)=10-14.c(OH-)=c(H+)=10-7mol/L, pH=7;水的电离是个吸热过程,若升高温度促进水的电离,水的pH<7。所以pH<7的溶液不一定是酸性溶液。错误。D.Al既能与酸反应放出氢气,也能与碱反应放出氢气。反应的方程式为: 2Al+6HCl=2AlCl3+3H2↑;2Al+2NaOH+2H2O=2NaAlO2+3H2↑。所以能与金属Al反应放出H2的溶液不一定是酸性溶液。错误。
H++OH-。在室温下在纯水中,c(OH-)・c(H+)=10-14.c(OH-)=c(H+)=10-7mol/L, pH=7;水的电离是个吸热过程,若升高温度促进水的电离,水的pH<7。所以pH<7的溶液不一定是酸性溶液。错误。D.Al既能与酸反应放出氢气,也能与碱反应放出氢气。反应的方程式为: 2Al+6HCl=2AlCl3+3H2↑;2Al+2NaOH+2H2O=2NaAlO2+3H2↑。所以能与金属Al反应放出H2的溶液不一定是酸性溶液。错误。
考点:考查溶液的酸碱性与pH的关系的知识。
本题难度:一般
3、填空题 Ⅰ(8分)PM2.5是连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样。测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
离子
| K+
| Na+
| NH4+
| SO42-
| NO3-
| Cl-
|
浓度/mol?L-1
| 4×10-6
| 6×10-6
| 2×10-5
| 4×10-5
| 3×10-5
| 2×10-5
根据表中数据判断PM2.5试样的pH 。
(2)NOx汽车尾气的主要污染物之一。汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:
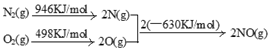
则N2和O2反应生成NO的热化学反应方程式为
(3)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如下:
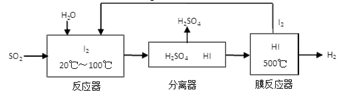
①用离子方程式表示反应器中发生的反应:
②将生成的氢气与氧气分别通入两个多孔惰性电极,KOH溶液作为电解质溶液,负极的电极反应式_ _
Ⅱ(10分)铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。工业上用铝土矿制备铝的某种化合物的工艺流程如下。
在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
(1)检验滤液B中是否还含有铁元素的方法为: (注明试剂、现象)。
(2)将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为 (填代号)。
A.氢氧化钠溶液 B.硫酸溶液 C.氨水 D.二氧化碳
(3)由滤液B制备氯化铝晶体涉及的操作为: 蒸发浓缩、冷却结晶、 、洗涤。
(4)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为 (填代号)。
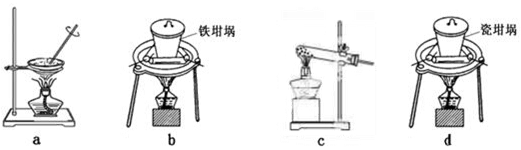
参考答案:Ⅰ(8分)(1)pH="4" 。
(2)N2(g)+O
本题解析:
试题分析:(1)溶液呈电中性,则n(H+)+n(K+)+n(Na+)+n(NH4+)=2n(SO42-)+n(NO3-)+n(Cl-)。所以c(H+)+ 4×10-6+6×10-6+2×10-5=2×4×10-5+3×10-5+2×10-5。解得c(H+)=1×10-4,所以pH=4;(2)根据题意N2和O2反应生成NO的热化学反应方程式为N2(g)+O2(g)= 2NO(g) △H="(946KJ/mol" +498KJ/mol― 2×630 KJ/mol)=+184kJ/mol;(3)①在反应器中SO2、I2、H2O发生反应产生硫酸和氢碘酸。用离子方程式表示为SO2+I2+2H2O=SO42-+2I-+4H+;②将生成的氢气与氧气分别通入两个多孔惰性电极,KOH溶液作为电解质溶液,通入氢气的电极是负极,负极的电极反应式是H2-2e-+2OH-=2H2O;Ⅱ(1)检验滤液B中是否还含有铁元素的方法为取少量滤液B,加入KSCN溶液,若不变红,再加入氯水,仍然不变红,说明滤液B 中不含铁元素。(2)由于在滤液B中的铝元素以Al3+形式存在,若使Al3+以沉淀形式析出,由于Al(OH)3是两性物质,既可以与强酸反应液可以与强碱发生反应,所以应该用弱碱,可选用的最好试剂为氨水,选项是C;(3)由滤液B制备氯化铝晶体涉及的操作为:加入浓盐酸蒸发浓缩、冷却结晶、过滤、洗涤,就得到了氯化铝晶体。(4)SiO2和NaOH焙烧制备硅酸钠,由于NaOH是强碱,能够与玻璃、陶瓷中的SiO2发生反应,所以应该用铁坩埚,可采用的装置为B。
考点:考查溶液的酸碱性、热化学方程式的书写、铁元素的检验、试剂的使用、仪器的选择的知识。
本题难度:困难
4、选择题 水的电离平衡曲线如图所示,下列说法不正确的是( )

A.图中五点KW间的关系:B>C>A=D=E
B.若从A点到D点,可采用:温度不变在水中加入少量的酸
C.若处在B点时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液显中性
D.若从A点到C点,可采用:温度不变在水中加入适量的NH4Cl固体
参考答案:D
本题解析:
试题分析:图中可知:从A点到C点,c(H+)=c(OH-),也就是说,是一个水的电离程度增大的过程,可以采用升温的方法来完成,温度不变在水中加入适量的NH4Cl固体,会使得溶液显酸性,而偏离C点,因此选D。
考点:考查水的电离的有关知识。
本题难度:一般
5、选择题 下列叙述正确的是
A.0.1mol・L-1氨水中,c (OH-)= c(NH4+)
B.10 mL 0.02mol・L-1HCl溶液与10 mL 0.02mol・L-1Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=10
C.在0.1mol・L-1CH3COONa溶液中,c(OH-)= c(CH3COOH)+c(H+)
D.0.1mol・L-1某二元弱酸强碱盐NaHA溶液中,
c(Na+)= 2c(A2-)+c(HA-)+c(H2A)
参考答案:C
本题解析:A.0.1mol・L-1氨水中,溶液显碱性,c (OH-)>c(H+),根据电荷守恒:c (OH-)= c(NH4+)+c(H+),c (OH-)>c(NH4+)。
B.10 mL 0.02mol・L-1HCl溶液与10 mL 0.02mol・L-1Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,很多同学错认为溶液的c (OH-)=  =0.01mol/L,pH=10,但忽略题目未涉及到温度,如果是非“常温下”,则计算是错误的; =0.01mol/L,pH=10,但忽略题目未涉及到温度,如果是非“常温下”,则计算是错误的;
D.0.1mol・L-1某二元弱酸强碱盐NaHA溶液中,电荷守恒:c(Na+)= 2c(A2-)+c(HA-)+c(OH-)。
点评:考查电解质溶液中守恒问题,离子浓度大小比较。
本题难度:简单
|