��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� 12mLŨ��Ϊ0.1mol��L-1Na2SO4��Һ��ǡ����40mLŨ��Ϊ0.01 mol��L-1K2Cr2O7��Һ��ȫ��Ӧ����Ԫ��Cr�ڱ���ԭ�IJ����еû��ϼ���
A��0
B��+2
C�� +3
D��+6
�ο��𰸣�C
�����������
�����Ѷȣ�һ��
2��ѡ���� ��һ�����������������������ɵ��γ�Ϊ���Ρ�����CaOCl2�����������¿��Բ����������û��� ��????????��
A��ˮ��Һ������
B�������ᷴӦ����1mol����ʱת��2mol����
C��ˮ��Һ����ʹ����-KI��ֽ����
D���Ⱥ����Ӽ��ֺ����ۼ�
�ο��𰸣�D
���������
�������������CaOCl2����CaCl2��Ca(ClO)2��ɵġ�CaCl2��ǿ��ǿ���Σ�ˮ��Һ�����ԣ�����Ca(ClO)2��ǿ�������Σ�ˮ��ʹˮ��Һ�Լ��ԡ�����B�������ᷴӦ��CaOCl2+H2SO4=CaSO4+Cl2��+H2O. ����1mol����ʱת��1mol����.����C��ˮ��Һ����ClO-����������ǿ�����ԣ��ܰ�I-����ΪI2��������ʹ����-KI��ֽ����������D�����������ӻ�����������Ӽ�����ClO-�к��м��Թ��ۼ�����˸û�����Ⱥ����Ӽ��ֺ����ۼ�����ȷ��2�����ʡ�
�����Ѷȣ�һ��
3������� ����ɫ�Լ���˫��ˮ����Ϊ��ҵ��Һ����������Ҫ�����ɿ�ҵ��Һ�е��軯���KCN������ѧ����ʽΪ��KCN+H2O2+H2O=A+NH3��
��1��������A�Ļ�ѧʽΪ??????????????????????????????
��2���ڱ�״������0.448L�������ɣ���ת�Ƶĵ�����Ϊ????????????????????
��3����Ӧ�б�������Ԫ��Ϊ??????????????????????????????
��4��H2O2����Ϊ��ɫ��������������?????????????????????????????????????
�ο��𰸣���1��KHCO3???��2��2.4��1022??��3��̼��C
�����������
�����Ѷȣ���
4������� MnO2��KMnO4������ѧ��ѧ�еij����Լ�����ش��������⣺
��1��MnO2��H2O2�ֽⷴӦ��������������MnO2�����ữ��H2O2��Һ�У�MnO2 �ܽ����Mn2+����Ӧ�����ӷ���ʽ��???????????????????????????????????????????????��
��2����MnO2��KMnO4�Ĺ���������ͼ

�������������Ͼ�Ϊ̼������ˮ��������Һ��K2MnO4�����绯�����MnO2��KMnO4��
��д��240������ʱ������Ӧ�Ļ�ѧ����ʽ??????????????????????????????????????��Ͷ��ʱ��������n(KOH)��n(MnO2) ???????????��
�������ĵ缫��ӦΪ???????????????????????????????????��
��B������?????????��д��ѧʽ����ͬ��������ѭ��ʹ�õ�������????????????????????��
�ܼ����ӽ���Ĥ��һ�ֲ����Ǿ۱�ϩ��أ�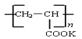 �����۱�ϩ��ص���Ľṹ��ʽΪ???????????��
�����۱�ϩ��ص���Ľṹ��ʽΪ???????????��
�������Ƶõ�KMnO4��Ʒ0.165 g��ǡ����0.335 g�������ữ��Na2C2O4��Ӧ��ȫ����KMnO4��
������???????????����ȷ��0.1%����
�ο��𰸣���1��MnO2 + 2H+ + H2O2 = Mn2+ +
���������
�����������1���������⣬��ϵ���غ㡢ԭ���غ㡢�����غ㣬�ɵ÷���ʽΪ��MnO2 + 2H+ + H2O2 = Mn2+ + O2 ��+ 2H2O����2������240������ʱMnO2��O2��KOH����������ԭ��Ӧ�����������غ㶨�ɺ͵����غ��֪ʶ��֪�����÷�Ӧ�Ļ�ѧ����ʽΪ��2MnO2 + O2 + 4KOH? �����Ѷȣ�һ��
�����Ѷȣ�һ��
5��ѡ���� ����˵����ȷ����
A��MnO2��4HCl(Ũ) MnCl2��Cl2����2H2O�У��������ͻ�ԭ�����ʵ���֮��Ϊ1��2
MnCl2��Cl2����2H2O�У��������ͻ�ԭ�����ʵ���֮��Ϊ1��2
B��2H2S��SO2��3S����2H2O�У���������ͻ�ԭ�������ʵ���֮��Ϊ1��1
C��3S��6KOH  2K2S��K2SO3��3H2O�У��������ͱ���ԭ����Ԫ������֮��Ϊ2��1
2K2S��K2SO3��3H2O�У��������ͱ���ԭ����Ԫ������֮��Ϊ2��1
D��5NH4NO3��4N2��2HNO3��9H2O�У���Ӧ�з���������Ӧ�ͷ�����ԭ��Ӧ�ĵ�Ԫ������֮��Ϊ5��3
�ο��𰸣���AD
���������
���������A��MnO2���ϼ۽�������������HCl���ϼ���������ԭ������4molHCl�μӷ�Ӧֻ��2mol������������A��ȷ��
B���ӷ�Ӧ��2molH2S����ԭ���������õ���������2molS��1molSO2������������ԭ�õ���ԭ����1molS������B����
C��3molS��Ӧ������2molS���ϼ۽��ͱ���ԭ������ԭ��Ӧ������1molS���ϼ����߱���������������Ӧ������C����
D����Ӧ��NH4+�е�N�ɩ�3������0�ۣ�����������Ӧ��NO3���е�N��+5�۽���0�ۣ�������ԭ��Ӧ������
�����Ѷȣ�һ��