微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质中,含极性键和非极性键且分子有极性的是(???? )
A.乙烯
B.H2O2
C.甲烷
D.三氯甲烷
参考答案:B
本题解析:
试题分析:乙烯是非极性分子,甲烷是含有极性键的非极性分子,三氯甲烷是极性分子,但不存在非极性键,所以答案选B。
点评:该题是高考中的常见考点,属于基础性试题的考查。试题侧重对基础知识的巩固和训练,有利于培养学生灵活运用基础知识解决实际问题的能力。该题的关键是明确极性键、非极性键、极性分子和非极性分子的含义以及判断依据。
本题难度:简单
2、填空题 (1)在下列物质中:①CO2??②KOH ??③He ??④BaSO4?⑤NaCl。其中只含有离子键的是(填序号,下同)??????????????????,既含有离子键又含有共价键的是??????????????????,不含化学键的是????????????????。
(2)下列物质在所述变化中:①烧碱熔化 ?②HCl气体溶于水 ?③NH4Cl受热分解 ?④干冰升华。其中化学键未被破坏的是(填序号,下同)?????????????,仅发生共价键破坏的是?????????????,既发生离子键破坏,又发生共价键破坏的是????????????????????。
参考答案:(1)⑤???②④????③???(2)④???②???③
本题解析:
试题分析:(1)①CO2含有极性共价键;②KOH含有离子键、极性共价键; ③He无化学键;④BaSO4含有离子键、极性共价键;⑤NaCl只含有离子键。因此只含有离子键的是⑤;既含有离子键又含有共价键的是②④;不含化学键的是③。(2)①烧碱熔化断裂离子键;②HCl气体溶于水破坏共价键;③NH4Cl受热分解既发生离子键破坏,又发生共价键破坏;④干冰升华破坏的是分子间作用力。因此其中化学键未被破坏的是④;仅发生共价键破坏的是②;既发生离子键破坏,又发生共价键破坏的是③。
本题难度:一般
3、选择题 甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)===CO2(g)+3H2(g);ΔH=+49.0 kJ・mol-1
②CH3OH(g)+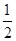 O2(g)===CO2(g)+2H2(g);ΔH=-192.9 kJ・mol-1
O2(g)===CO2(g)+2H2(g);ΔH=-192.9 kJ・mol-1
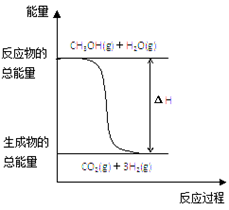
下列说法正确的是
A.若用甲醇(CH3OH)为原料设计成燃料电池,则通入甲醇的电极为正极
B.反应①中的能量变化如上图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应:CH3OH(l)+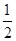 O2(g)===CO2(g)+2H2(g) 的ΔH>-192.9 kJ・mol-1
O2(g)===CO2(g)+2H2(g) 的ΔH>-192.9 kJ・mol-1
参考答案:D
本题解析:
试题分析:A、若用甲醇(CH3OH)为原料设计成燃料电池,甲醇发生氧化反应,则通入甲醇的一极是负极,错误;B、反应①是吸热反应,反应物的总能量低于生成物的总能量,错误;C、若以②的方式甲醇转化为氢气,则该过程放热,错误;D、液态甲醇转化为气态甲醇需要吸收热量,所以液态甲醇完全燃烧放出的热量低于气态甲醇放出的热量,ΔH<0,则ΔH>-192.9 kJ・mol-1,正确,答案选D。
考点:考查化学反应的热效应的判断,电化学原理的应用
本题难度:一般
4、填空题 2SO2(g)+O2 (g)= 2SO3 (g),反应过程的能量变化如图所示。已知:1 mol SO2(g)氧化为1 mol SO3(g)的ΔH="-99" kJ/mol。
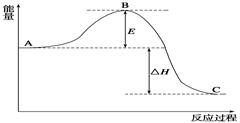
请回答下列问题:
(1)图中A、C分别表示????????????、 ???????????????,E的大小对该反应的反应热有无影响? ???????。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?????????,理由是?????????????????????????????????????????????????????????????;
(2)图中ΔH= ????????????kJ/mol;
(3)如果反应速率v(SO2)为0.05 mol/(L・min),则v(O2)= ????????????????mol/(L・min);
(4)已知单质硫的燃烧热为296 kJ/mol,计算由S(s)生成3 mol SO3(g)的ΔH(要求计算过程)。
参考答案:(1)反应物能量?生成物能量?没有影响?降低??因为催化剂改
本题解析:
试题分析:(1)根据图像可知,图中A、C分别表示反应物能量和生成物能量。E为活化能,与反应热无关,但使用催化剂可以降低活化能。
(2)图中表示的是2molSO2的反应,因此△H=-99×2kJ/mol=-198 kJ/mol.
(3)依据速率之比等于化学计量数之比可知,v(O2)=0.05 mol/(L・min)÷2=0.025 mol/(L・min).
(4)S(s)+O2(g)=SO2 (g)??? ΔH1=-296 kJ/mol??①
SO2(g)+ O2(g)=SO
本题难度:一般
5、选择题 下列说法正确的是
A.干冰升华要吸收大量的热,这就是化学反应中的吸热反应
B.凡是在加热或点燃条件下进行的反应都是吸热反应
C.人们用氢氧焰焊接或切割金属,主要是利用了氢气和氧气化合时所放出的能量
D.明矾有净水作用,所以用明矾处理硬水,可以使硬水软化
参考答案:C
本题解析:
试题分析:
A、干冰升华是物理变化,不属于吸热反应,故A错误;
B、有些放热反应也需要一定的引发条件才能进行,如氢气在氧气中燃烧需要点燃,故B错误;
C、氢气和氧气化合时所放出的大量的能量,可焊接或切割金属,故C正确;
D、明矾可以净水,其净水原理是铝离子水解形成氢氧化铝胶体吸附悬浮颗粒,不能吸附溶于水的钙、镁离子,故不能软化水,故D错误。
考点:考查化学反应中能量的变化、明矾净水的原理
点评:本题考查了化学反应中能量的变化、明矾净水的原理,难度不大。注意掌握常见的放热反应和吸热反应。
本题难度:一般