微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
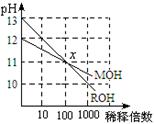
1、选择题 MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如右图?所示。下列叙述中不正确的是
 ?
?
A.MOH是一种弱碱
B.在x点,c(M+) =c(R+)
C.在x点,ROH完全电离
D.稀释前,c(ROH) =10 c(MOH)
参考答案:D
本题解析:
试题分析:根据图像可知,稀释100倍后,ROH的pH变化由13变为11,而MOH的则由12变为11,因此MOH是弱碱,存在电离平衡。ROH是强碱,A和C都是正确的;根据电荷守恒可知,B正确;D不正确,弱碱存在电离平衡,应该是c(ROH)<10 c(MOH),答案选D。
点评:在比较溶液中离子浓度大小时,应该注意利用好几个守恒关系,即电荷守恒、物料守恒和质子守恒都能够。
本题难度:一般
2、简答题 醋酸是日常生活中最常见的调味剂和重要的化工原料,醋酸钠、醋酸铵是其常见的盐,已知醋酸铵溶液呈中性.请回答:
(1)常温下,向1L0.1mol/L的醋酸溶液中加入0.1mol醋酸钠固体,则醋酸的电离平衡向______(填“正”或“逆”)反应方向移动,溶液中
c(CH3COO-)?c(H+)
c(CH3COOH)
的值______(填“增大”、“减小”或“不变”).此时测得溶液pH<7,则溶液中各离子浓度的大小顺序是______;
(2)下列说法中,正确的是______(填字母);
a.CH3COOH溶液加水稀释后,溶液中c(CH3COOH)
c(CH3COO-)c(H+)
的值减小
b.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同
c.升高温度可以促进醋酸电离,也能够促进醋酸钠水解
(3)常温下amol/LCH3COOH稀溶液和bmol/LKOH稀溶液等体积混合,下列判断一定错误的是______.
a.若c(OH-)>c(H+),a=b
b.若c(K+)>c(CH3COO-),a>b
c.若c(OH-)=c(H+),a>b
d.若c(K+)<c(CH3COO-),a<b.
参考答案:(1)在醋酸溶液中存在电离平衡:CH3COOH?CH3COO
本题解析:
本题难度:简单
3、计算题 在25℃下,将a mol・L-1的氨水与0.01mol・L-1的盐酸等体积混合后,溶液中c(NH4+)=c(Cl-)。试用含a的代数式计算NH3・H2O的电离常数Kb。
参考答案: 本题解析:略 本题解析:略
本题难度:简单
4、选择题 下列溶液中加入少量NaOH固体导电能力变化不大的是( )
A.NH3・H2O
B.CH3COOH
C.盐酸
D.H2O
参考答案:C
本题解析:
AD中,NaOH溶于水,离子浓度增大,导电能力增强;B中CH3COOH是弱电解质,与NaOH反应后生成CH3COONa是强电解质,离子浓度增大,导电能力增强;HCl强电解质,与NaOH反应后生成NaCl,也是强电解质,离子浓度变化不大。故选C
本题难度:一般
5、简答题 (1)体积相同,浓度均为0.2mol/L的盐酸和CH3COOH溶液,分别加水稀释10倍,溶液的pH分别变成m和n,则m与n的关系为______,稀释后两溶液中和NaOH溶液的能力______.
(2)体积相同,pH均等于3的盐酸和CH3COOH溶液,分别加入等浓度的NaHCO3的溶液,开始时放出二氧化碳的速率盐酸______醋酸(填“大于”“等于”“小于”)
(3)常温下,将pH=2的盐酸和pH=12的氨水等体积混合,混合后溶液的pH______7(填“大于”“等于”“小于”).并解释你所填选项的理由______.
(4)如何证明醋酸是弱酸?______.
参考答案:(1)HCl、CH3COOH都是一元酸,但HCl是强酸,醋酸
本题解析:
本题难度:简单
|
|