微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 已知H2A在水中存在以下平衡:H2A H++HA-,HA-
H++HA-,HA- H++A2-。回答以下问题:
H++A2-。回答以下问题:
(1)已知常温下,H2A的钙盐(CaA)饱和溶液中存在平衡:
CaA(s) Ca2+(aq)+A2-(aq) ΔH > 0。
Ca2+(aq)+A2-(aq) ΔH > 0。
①温度升高时,Ksp________(填“增大”、“减小”或“不变”下同)。
②滴加少量浓盐酸,c (Ca2+)________,原因是____???______________(用文字和离子方程式说明)。
(2)若向CaA悬浊液中加入CuSO4溶液,生成一种黑色固体物质,写出该过程中反应的离子方程式______________________。若某CuSO4溶液中c (Cu2+)=0.02 mol/L,如果要生成Cu(OH)2沉淀,应调整溶液pH,使之大于________(已知Ksp[Cu(OH)2]=2.0×10-20)。
(3)常温下,向某纯碱溶液中滴入酚酞,溶液呈红色,则该溶液呈________性。在分析该溶液遇酚酞呈红色的原因时,甲同学认为是配制溶液时所用的纯碱样品中混有NaOH所致;乙同学认为是溶液中电离出的CO32-水解所致,请你设计一个简单的实验方案给甲和乙两位同学的说法进行评判(包括简要操作、现象和结论)_________________ ___________。
参考答案:(1)①增大;②增大, 加盐酸发生反应:A2-+H+
本题解析:
试题分析:(1)已知常温下,H2A的钙盐(CaA)饱和溶液中存在平衡:CaA(s)? ?Ca2+(aq)+A2-(aq) ΔH > 0。①该反应为吸热反应,温度升高,平衡正向移动,Ksp增大;②根据化学平衡移动原理,滴加少量浓盐酸,发生反应:A2-+H+
?Ca2+(aq)+A2-(aq) ΔH > 0。①该反应为吸热反应,温度升高,平衡正向移动,Ksp增大;②根据化学平衡移动原理,滴加少量浓盐酸,发生反应:A2-+H+ 本题难度:一般
本题难度:一般
2、选择题 在醋酸与氢氧化钠溶液的反应过程中,溶液中的相关离子浓度呈现出下列排列顺序: c(CH3COO-)>c(Na+)>c(H+)>c(OH-)。满足该条件的反应是
A.0.01mol・L-1的CH3COOH与pH=12的NaOH溶液等体积混合
B.0.2 mol・L-1的CH3COOH溶液与0.1 mol・L-1的NaOH溶液等体积混合
C.CH3COOH溶液与NaOH溶液混合后所得溶液的pH=7
D.0.1 mol・L-1的CH3COOH溶液与等物质的量浓度、等体积的NaOH溶液混合
参考答案:B
本题解析:A错,0.01mol・L-1的CH3COOH与pH=12的NaOH溶液等体积混合,混合后溶液中溶质为醋酸钠,溶液中离子浓度大小关系为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+);B正确;C错,CH3COOH溶液与NaOH溶液混合后所得溶液的pH=7即得c(CH3COO-)=c(Na+)>c(H+)=c(OH-);D错,.0.1 mol・L-1的CH3COOH溶液与等物质的量浓度
本题难度:一般
3、选择题 下列叙述不正确的是
A.相同物质的量浓度的①CH3COONa溶液②NaNO3溶液③NH4Cl溶液④NaOH溶液,pH的大小顺序是:④>①>②>③
B.在Na2SO3和NaHSO3混合液中:c(Na+)+c(H+)=c(HSO3-)+c(OH-)+2c(SO32-)
C.相同条件下,pH=10的CH3COONa溶液和氨水中,由水电离出的c(OH-)前者大于后者
D.某溶液中只含Na+、CH3COO-、H+、OH-四种离子,则溶液一定呈现碱性
参考答案:D
本题解析:
试题分析:A、CH3COONa水解显碱性,NaOH为强碱,NaNO3为中性,NH4Cl水显酸性,所以pH的大小顺序为:④>①>②>③,正确;B、在Na2SO3和NaHSO3混合液中,根据电荷守恒可得:c(Na+)+c(H+)=c(HSO3-)+c(OH-)+2c(SO32-),正确;C、CH3COONa促进水的电离,氨水抑制水的电离,所以相同条件下,pH=10的CH3COONa溶液和氨水中,由水电离出的c(OH-)前者大于后者,正确;D、某溶液中只含Na+、CH3COO-、H+、
本题难度:一般
4、选择题 0.02mol・L―1的HCN溶液与0.02mol・L―1的NaCN溶液等体积混合,已知混合溶液中C(CN-)<C(Na+),则下列关系中,正确的是:
A.C(Na+)>C(CN-)>C( H+)>C(OH-)
B.C(HCN)+C (CN-)=0.04mol・L-1
C.C(CN-)>C(HCN)
D.C(Na+)+C(H+)= C(CN-)+C(OH-)
参考答案:D
本题解析:设以100L等体积混合,即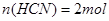 ;
;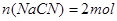 溶合后,根据电荷守恒得
溶合后,根据电荷守恒得 本题难度:一般
本题难度:一般
5、选择题 用物质的量均是0.1 mol的CH3COOH和CH3COONa配成1L混合溶液,已知其中c(CH3COO-)大于c(Na+),对该混合溶液的下列判断正确的是(???)
A.c(CH3COOH)>c(CH3COO-)
B.c(CH3COO-)+c(CH3COOH)=0.1 mol・L-1
C.c(H+)>c(OH-)
D.c(CH3COO-)+c(OH-)=0.1 mol・L-1
参考答案:C
本题解析:c(CH3COO-)大于c(Na+),所以根据电荷守恒定律可知,溶液显酸性。这说明醋酸的电离程度大于醋酸钠的水解程度,因此C正确,A不正确,应该是c(CH3COOH)<c(CH3COO-) ;B不正确,应该是c(CH3COO-)+c(CH3COOH)=0.2 mol・L-1;D不正确,应该是c(CH3COO-)+c(OH-)>0.1 mol・L-1,所以答案选C。
本题难度:一般