微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 鉴别乙醇、乙醛、乙酸应选用的试剂最好是?????????????(??)
A.Na2CO3溶液
B.汽油
C.水
D.新制Cu(OH)2悬浊液
参考答案:D
本题解析:乙醛含有醛基,能被新制的氢氧化铜悬浊液氧化,而乙酸含有羧基,能溶解氢氧化铜,因此和氢氧化铜不反应,所以答案选D。
本题难度:一般
2、选择题 下列实验所推出的结论不正确的是(???? )

A.向漂白粉中加入稀盐酸,有无色无味气体产生,则说明漂白粉已变质
B.用丁达尔现象可鉴别FeCl3溶液和Fe(OH)3胶体
C.溶液里加入盐酸,有能使澄清石灰水变浑浊的无色无味的气体生成,则说明溶液中一定含有HCO3-
D.溶液中加入稀硝酸后,再加少量AgNO3溶液,有白色沉淀生成,则溶液中含有Cl-
参考答案:C
本题解析:
试题分析:A中说明漂白粉中含有碳酸钙,已经变质,正确;胶体可以产生丁达尔效应,但溶液不能,据此可以鉴别二者,B正确;C不正确,也可能含有CO32-;D正确,答案选C。
点评:该题是中等难度的试题,也是高考中的常见题型。试题贴近高考,注重能力的培养和解题方法的训练,有利于培养学生的逻辑思维能力。该题学生需要明确的是进行物质的检验时,要依据物质的特殊性质和特征反应,选择适当的试剂和方法,准确观察反应中的明显现象,如颜色的变化、沉淀的生成和溶解、气体的产生和气味、火焰的颜色等,进行判断、推理、验证即可。
本题难度:一般
3、填空题 (14分)铬铁矿的主要成分可表示为FeO・Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,以下是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的流程图:

已知:①4FeO?Cr2O3+8Na2CO3+7O2 8Na2CrO4+2Fe2O3+8CO2↑;
8Na2CrO4+2Fe2O3+8CO2↑;
②Na2CO3+Al2O3 2NaAlO2+CO2↑;
2NaAlO2+CO2↑;
③Cr2CO72-+H2O 2CrO42-+2H+
2CrO42-+2H+
根据题意回答下列问题:
(1)固体X中主要含有??????(填写化学式);要检测酸化操作中溶液的pH是否等于4.5,应该使用?? ______________???(填写仪器或试剂名称)。
(2)酸化步骤用醋酸调节溶液pH<5,其目的是? _______________________ 。
(3)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、?????????、过滤、???????、干燥。
(4)下表是相关物质的溶解度数据,操作III发生反应的化学方程式是:Na2Cr2O7 + 2KCl=K2Cr2O7 ↓+ 2NaCl,该反应在溶液中能发生的理由是_____________________________。
物质
| KCl
| NaCl
| K2Cr2O7
| Na2Cr2O7
|
溶解度(g/100g水)
| 0℃
| 28
| 35.7
| 4.7
| 163
|
40℃
| 40.1
| 36.4
| 26.3
| 215
|
80℃
| 51.3
| 38
| 73
| 376
?
(5)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是称取n g样品,加入过量??????? ____?(填写试剂)、溶解、过滤、再???????(填写试剂)、……灼烧、冷却、称量,得干燥固体m g。计算祥品中氢氧化铝的质量分数为????(用含m、n的代数式表示)。
参考答案:(13分)(1)Fe2O3、MgO(2分)PH计或pH试纸(
本题解析:
试题分析:(1)铬铁矿的主要成分可表示为FeO?Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,加入氧气和碳酸钠,发生反应为:①4FeO?Cr2O3+8Na2CO3+7O2 8Na2CrO4+2Fe2O3+8CO2↑、②Na2CO3+Al2O3 8Na2CrO4+2Fe2O3+8CO2↑、②Na2CO3+Al2O3 2NaAlO2+CO2↑、③Cr2CO72-+H2O 2NaAlO2+CO2↑、③Cr2CO72-+H2O 2CrO42-+2H+,操作Ⅰ是过滤得到固体X为Fe2O3、MgO;要检测酸化操作中溶液的pH是否等于4.5,普通pH试纸只能测定溶液pH到整数,是近似测定,准确测定需要用pH计或精确pH试纸; 2CrO42-+2H+,操作Ⅰ是过滤得到固体X为Fe2O3、MgO;要检测酸化操作中溶液的pH是否等于4.5,普通pH试纸只能测定溶液pH到整数,是近似测定,准确测定需要用pH计或精确pH试纸;
(2)酸化步骤用醋酸调节溶液pH<5,依据流程图中物质的转化和制备目的可知,结合反应平衡Cr2O72-+H2O 2CrO42-+2H+,加入酸,氢离子浓度增大,平衡左移,作用是使CrO42-转化为Cr2O72--; 2CrO42-+2H+,加入酸,氢离子浓度增大,平衡左移,作用是使CrO42-转化为Cr2O72--;
(3)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩,冷却结晶、过滤、洗涤、干燥得到晶体;
(4)依据图表物质的溶解度分析对比,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl=K2Cr2O7↓+2NaCl,这说明K2Cr2O7的溶解度比Na2Cr2O7小(或四种物质中K2Cr2O7的溶解度最小);
(5)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是先利用氢氧化铝的两性,用氢氧化钠溶液溶解氢氧化铝过滤得到滤液中通入二氧化碳生成氢氧化铝沉淀,灼烧干燥得到氧化铝干燥固体m g,依据铝元素守恒计算,样品中氢氧化铝的质量分数= ×100%= ×100%=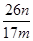 。 。
本题难度:困难
4、填空题 为了除去KCl溶液中少量的MgCl2、MgSO4,可选用Ba(OH)2、HCl和K2CO3三种试剂,按下图步骤操作:

(1)写出三种试剂的化学式:A??????????????,B??????????????,C??????????????。
(2)加过量A的原因是????????????????????????????????????????????????????
有关反应的化学方程式为:??????????????????????????????????????????????????????????????????????????????
(3)加过量B的原因是:??????????????????????????????????????????????? ???? ????
有关反应的化学方程式为:????????????????????????????????????????????????????????????????????????????
参考答案:(1)写出三种试剂的化学式:A :Ba(OH)2,? B :
本题解析:略
本题难度:简单
5、填空题 (8分)有A、B、C、D、E、F六种化合物,它们在水溶液中反应关系如下:
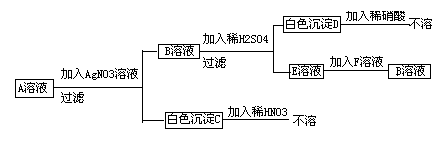
⑴试推断各物质的化学式:A?????,B???????????,C???????,D??????????,E???????,F???????。
⑵写出A溶液与硝酸银溶液反应的化学方程式:?????????????????????????????????
参考答案:(1)BaCL2(2) Ba(NO)3(3)AgCl (4)
本题解析:考查物质鉴别和检验及方程式的书写。A和硝酸银反应生成的白色沉淀C,不能溶于硝酸中,说明C是氯化银,则A中含有氯离子;溶液B和稀硫酸反应又生成不溶于硝酸的白色沉淀,因此D是硫酸钡,则B中含有Ba2+,则A就是氯化钡,B是硝酸钡,E是硝酸。由于E能和F反应生成硝酸钡,实验F是氢氧化钡。其中氯化钡和硝酸银反应的方程式是BaCl2+2AgNO3=2AgCl+Ba(NO3)2.
本题难度:一般
|