��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
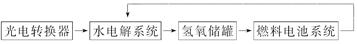
1��ѡ���� ����ͼ��ʾ��ij̫�տռ�վ����ת��ϵͳ�ľֲ�ʾ��ͼ������ȼ�ϵ�ز���KOH��ҺΪ���Һ�������й�˵������ȷ����(? )
 ???
???
������ʱ????????????������ʱ
A��������ת��ϵͳ����ʱ���費�ϲ���H2O
B����ת��ϵͳ��������������Դ��̫����
C��ˮ���ϵͳ�е�������Ӧ��O2��2H2O��4e��=4OH��
D��ȼ�ϵ�طŵ�ʱ�ĸ�����Ӧ��H2��2e��=2H��
�ο��𰸣�B
���������ˮ���ʱ����Ϊ2H����2e��=H2����C�����ȼ�ϵ�طŵ�ʱ����ΪH2��2OH����2e��=2H2O����D�����A����H2O����ѭ�����ã�����B����ȷ��
�����Ѷȣ�һ��
2������� ��9�֣���Ҫ�����ͼ���������б�Ҫ�����Ӳ���գ�
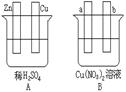
��1����Aͼ�У�ʹͭƬ��ðH2���ݡ�����Ա�Ҫ���ӣ������Ӻ��װ�ý�????????????????���缫��Ӧʽ��
п�壺??????????????????��ͭ�壺??????????????????��
��2����Bͼ�У�a�� b����ʯī�缫��ʹa������ͭ����b������???�����Ա�Ҫ�����Ӻ缫��Ӧʽ��a����???????????????????????????????b����?????????????????????????????������һ��ʱ���ֹͣ��Ӧ�����һ������????????����Һ�ָܻ�������ǰ��ȫһ�¡�
�ο��𰸣���1�� �����������1��ҪʹͭƬ�ϲ������ݣ���Ӧ�ù���ԭ��أ�п�Ǹ�����ʧȥ���ӡ�ͭ����������Һ�е��������������õ����ӣ��缫��ӦʽΪп�壺Zn-2e- =Zn2��ͭ�壺2H����2e-��H2����
�����������1��ҪʹͭƬ�ϲ������ݣ���Ӧ�ù���ԭ��أ�п�Ǹ�����ʧȥ���ӡ�ͭ����������Һ�е��������������õ����ӣ��缫��ӦʽΪп�壺Zn-2e- =Zn2��ͭ�壺2H����2e-��H2����
��2��ʹa������ͭ��Ӧ�ù��ɵ��أ�����a��������������b����������b��OH���ŵ磬�����������缫��Ӧʽ�ֱ���a����Cu2����2e- =Cu��b����4OH�D�D4e����O2����2H2O�����ڴ���Һ�м��ٵ���ͭ������������Ӧ�ü�������ͭ���ָܻ������ǰ��״̬��
�����Ѷȣ���
3��ѡ���� ������ʵ�����õ绯ѧ���۽��͵���????????????????????????????????��????��
A���ִ�ˮ���´�����װ��һ��������п��
B����п�ȴ�п��H2����
C����п���ȶ���������
D�����ʽ��³��ڷ��ú�����䰵
�ο��𰸣�D
���������A����������������������������п�к������ʣ����Թ���ԭ��ؼӿ췴Ӧ���ʡ�������˳����п�������������Ʋ�������п����������ʴ��п�Ǹ����������������ʽ��³��ڷ��ú�����䰵���������Ļ�ѧ��ʴ�������ǵ绯ѧ��ʴ������D��
�����Ѷȣ�һ��
4��ѡ���� �����й����������漰�IJ�����ԭ��˵����ȷ���� [???? ]
A���ϳɰ����������н�NH3Һ�����룬�ɼӿ�����Ӧ���ʣ����N2��H2��ת����
B��������п����п���Դ������������ƹ�����Ҫ���Ƶ���ǿ�ȡ���ҺpH������
C��������ǰ���п���Dz��������������������������Ӷ�����������ʴ����
D����⾫��ͭʱ�������ܽ�ͭ������������������ͭ�����������
�ο��𰸣�C
���������
�����Ѷȣ�һ��
5������� ��12�֣�����������ԭ��Ӧ��2Fe3+(aq)��Fe(s)��3Fe2+(aq)�����ԭ��ز������ͼ��ʾʵ�顣��ش��������⣺

�ŵ缫X�IJ�����????????????��ʯī�缫Ϊ��ص�???????????����
��Bװ���з����ĵ缫��Ӧ����ʽΪ????????????????????????????????????��������������Na2SO4��������?????????????????????????????????��
��ͭ˿b����ֽ�Ӵ���������Ϊ??????????????????????????????���˴��缫��Ӧ����ʽΪ��??????????????????????????????��
�ο��𰸣���1����??��???��2��Fe3++e��=Fe2+??��ǿ��
�����������1�����ݷ�Ӧʽ��֪�������ӵõ����ӣ�������������ʧȥ���ӣ��ǻ�ԭ��������A����Һ���Ȼ�����������X�缫������ʯī�缫��������
��2��ԭ����������õ����ӣ�����B��������Ӧʽ��Fe3++e��=Fe2+����������ǿ����ʣ���������������ǿ��Һ�ĵ����ԡ�
��3��ͭ˿b�͵�Դ�ĸ�������������������Һ�е������ӷŵ磬�����������缫��Ӧʽ��2H++2e-=H2�������������ӷŵ磬�ƻ���������Χˮ�ĵ���ƽ�⣬����������Χ��Һ�Լ��ԣ�����ֽ��Ϊ��ɫ��
�����Ѷȣ�һ��