微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 一定温度下,溴化银在水中的沉淀溶解平衡曲线如下图。下列说法正确的是
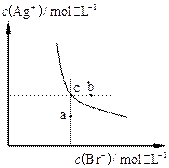
A.向溴化银的浊液中加入溴化钠溶液,
溴化银的Ksp减小
B.图中a点对应的是不饱和溶液
C.向c点的溶液中加入0.1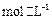
 ,则
,则 减小
减小
D.升高温度可以实现c点到b点的转化
参考答案:BC
本题解析:略
本题难度:一般
2、选择题 将AgCl与AgBr的饱和溶液等体积混合,再加入足量浓AgNO3溶液,发生的反应为[???? ]
A.只有AgBr沉淀生成
B.AgCl和AgBr沉淀等量生成
C.AgCl和AgBr沉淀都有,但以AgCl沉淀为主
D.AgCl和AgBr沉淀都有,但以AgBr沉淀为主
参考答案:C
本题解析:
本题难度:一般
3、选择题 常温下,Ksp(CaCO3)=4.96×10-9,Ksp(MgCO3)=6.82×10-6。含有MgCO3沉淀的MgCl2溶液中,已知c(Mg2+)="0.2" mol/L。如果加入等体积的CaCl2溶液,若要产生CaCO3沉淀,加入CaCl2溶液的物质的量浓度最小约为
A.7.27×10-5mol/L
B.1.45×10-4mol/L
C.2.9×10-4mol/L
D.5.8×10-4mol/L
参考答案:B
本题解析:
试题解析:两溶液等体积混合,所以MgCl2溶液中c(Mg2+)="0.1" mol/L,利用Ksp(MgCO3)=c(Mg2+)×c(CO32-)=6.82×10-6,解得c(CO32-)=6.82×10-5mol/L ,再根据Ksp(CaCO3)=c(Ca2+)×c(CO32-)=4.96×10-9,解得c(Ca2+)=7.27×10-5mol/L,则原溶液中c(Ca2+)=2×7.27×10-5mol/L=1.45×10-4mol/L ,故B正确。
考点:Ksp的应用
本题难度:一般
4、选择题 下列实验不能达到目的的是
选项
| 实验操作
| 实验目的
|
A
| 向5 mL 0.1 mol/L AgNO3溶液中滴加3滴0.1 mol/LNaCl溶液,产生白色沉淀;再向其中滴加3滴0.1mol/L的KI溶液,有黄色沉淀产生
| 验证Ksp(AgCl)> Ksp(AgI)
|
B
| 向适量样品溶液中滴加KSCN溶液
| 检验FeSO4溶液是否被氧化
|
C
| 向适量样品溶液中滴加盐酸酸化,再滴加BaCl2溶液
| 检验Na2SO3溶液是否被氧化
|
D
| 向Na2SiO3溶液中通入CO2
| 验证非金属性:碳>硅
参考答案:A
本题解析:A中滴加的NaCl不能使溶液中Ag+完全沉淀,因而不能得到Ksp(AgCl)> Ksp(AgI)的结构;如果加入KSCN溶液显红色,可以证明Fe2+被氧化了;先加盐酸酸化,如果没有现象,再加氯化钡溶液,产物白色沉淀,则证明有SO42-,可以检验FeSO4溶液是否被氧化;向向Na2SiO3溶液中通入CO2,是高价含氧酸间的强酸制弱酸,可以证明非金属性:碳>硅。
本题难度:一般
5、选择题 向AgCl饱和溶液中加水,下列叙述正确的是 [???? ]
A.AgCl的溶解度增大
B.AgCl的溶解度、Ksp均不变
C.AgCl的Ksp增大
D.AgCl的溶解度、Ksp均增大
参考答案:B
本题解析:
本题难度:一般
|