��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����ϼ�Ϊ+5�۵�AԪ�ص�ij��������������ػ�ԭ�������0.003Ħ+5�۵�AԪ�ر���ԭΪ�ϵͼ�̬������0.5mol/L�����������Һ15ml����AԪ�ر���ԭ��Ļ��ϼ��ǣ�??��
A����2
B��0
C��+4
D��+2
�ο��𰸣�B
���������������ص����ʵ�����0.0075mol��ʧȥ���ӵ����ʵ�����0.0075mol��2��0.015mol�����Ը��ݵ��ӵĵ�ʧ�غ��֪��1molA�õ��ĵ��ӵ����ʵ�����0.015��0.003��5mol������AԪ�ر���ԭ��ļ�̬��0�ۣ���ѡB��
�����Ѷȣ�һ��
2������� KClO3��Ũ������һ���¶��·�Ӧ�����̻�ɫ���ױ���ClO2����仯�ɱ���Ϊ��
______KClO3+______HCl��Ũ����______KCl+______ClO2��+______Cl2��+____________
��1������ɸû�ѧ����ʽƽ��ƽ��δ֪�ﻯѧʽ��ϵ����������
��2��Ũ�����ڷ�Ӧ����ʾ������������______
��ֻ�л�ԭ�Ԣڻ�ԭ�Ժ�����
��ֻ�������Ԣ������Ժ�����
��3��ClO2���к�ǿ�������ԣ���ˣ�����������������������Ч�ʣ��Ե�λ�����õ��ĵ�������ʾ����Cl2��______����
�ο��𰸣���1��������ԭ��Ӧ�л��ϼ۲����棬����������е���Ԫ�ػ��ϼ�
���������
�����Ѷȣ���
3��ѡ���� ��֪P������KOH��Һ�еı仯�ǣ�4P+3KOH+3H2O=3KH2PO2+PH3��������˵����ȷ����
A������PH3���������е�ԭ�ӿ��ܹ�ƽ�桡
B���÷�Ӧ��P����ԭ����H2O��������
C�����Ԫ�صĵ�һ�����ܵĴ�С˳��S��P��Si
D���÷�Ӧÿ����0.3Ħ������ת�ƣ�PH3�����о���0.3Ħ��P��H���γ�
�ο��𰸣�D
���������
���������A��PH3����Ӧ�ú�NH3����һ����Ϊ�����Σ� ���������е�ԭ�Ӳ����ܹ�ƽ�棬����B���÷�Ӧ��P����(0��)��һ����ת��ΪKH2PO2(����PΪ+1��)��һ����ת��ΪPH3 (����PΪ-3��)������Ԫ�ؼ�̬δ�ı䣬����P���ʼ��������������ǻ�ԭ��������C�����Ԫ�صĵ�һ�����ܵĴ�С˳��ӦΪ�� P��S��Si��ͬ���ڵڢ�A>�ڢ�A��������D��ÿ����һ��PH3���ӣ���������3��P��H����ת��3e-���÷�Ӧÿ����0.3Ħ������ת�ƣ�PH3�����о���0.3Ħ��P��H���γɣ���ȷ��
�����Ѷȣ�һ��
4������� Fe3P��ϡHNO3��Ӧ����Fe(NO3)3��NO��H3PO4��H2O��
(1) д����Ӧ�Ļ�ѧ����ʽ��_______________________________________��
(2) ������Ӧ�У�������1.8 mol Fe3+ʱ���ų�NO�����(��״����)��__________L�����ĵ�HNO3��__________mol��
(3) ������Ӧ�У�����21 mol���ӷ���ת��ʱ������H3PO4��_________mol������ԭ��HNO3��___________g��
�ο��𰸣�(1) 3Fe3P��41HNO3��ϡ����9Fe(N03)3��
�����������1�����ݷ�Ӧ����������֪��Fe3Pʧȥ14�����ӡ����ᵱ��ԭ������NO������õ�3�����ӣ������������ͻ�ԭ�������ʵ���֮����14�U3����˷�ӦʽΪ3Fe3P��41HNO3��ϡ����9Fe(N03)3��14NO����3H3PO4��16H2O��
��2�����ݷ���ʽ��֪��������1.8 mol Fe3+ʱ������NO��
�����Ѷȣ�һ��
5��ѡ���� a mol FeS��b mol FeOͶ�뵽V L��c mol��L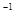 ��������Һ�г�ַ�Ӧ������NO���壬���ó�����Һ�ɷֿɿ�����Fe��NO3��3��H2SO4�Ļ��Һ����Ӧ��δ����ԭ���������Ϊ
��������Һ�г�ַ�Ӧ������NO���壬���ó�����Һ�ɷֿɿ�����Fe��NO3��3��H2SO4�Ļ��Һ����Ӧ��δ����ԭ���������Ϊ
�٣�a+b����63 g????????????????�ڣ�a+b����189 g
�ۣ�a+b�� mol??????????????????��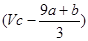 mol
mol
A���٢�
B���ڢ�
C���٢�
D���ڢ�
�ο��𰸣�D
���������
���������FeS��FeO�ڷ�Ӧ�й�ʧȥ���ӵ����ʵ����ǣ�a��8a��b��mol�����Ա���ԭ��������ʵ�����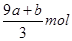 ����û�б���ԭ����������ʵ�����
����û�б���ԭ����������ʵ�����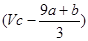 �����Ѷȣ�һ��
�����Ѷȣ�һ��