微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (6分) 为了在实验室制取干燥的氨气,甲、乙、丙三位同学分别设计了如下三套实验装置
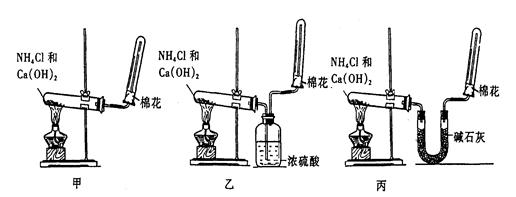
(1)实验装置和所用药品都正确的是(填“甲”、“乙”或“丙”)????。
(2)写出制取氨气的化学方程式??????????????????????????????????。
(3)如何检验氨气是否收集满(简述操作方法、现象和结论)??????????。
(4)氨是一种重要的化工产品,其化学式为????????????,具有??????????????气味,密度比空气?????????????。
参考答案:
(1)丙
(2) 本题解析:略
本题解析:略
本题难度:简单
2、实验题 (13分)下图所示装置进行有关实验,将A逐滴加入B中

⑴若A是实验室的一种常用燃料,B是生石灰,实验中观察到C中黑色固体逐渐变红,当C中黑色固体大部分变红时,关闭F,然后往烧杯中加入热水,静止一会,观察到III中试管壁出现了光亮的银镜,则A是?????????????,C是????????????????,请写出反应管C中所发生的反应方程式:??????????????????????????????????????????????????。试管E中所发生反应的离子方程式:????????????????????????????????????????????。
⑵若I处酒精灯不加热, B、C仍是实验(1)中原物质,实验中也观察到C中黑色固体逐渐变红,同时可观察到E中溶液先形成沉淀,然后沉淀溶解,并有一种无色无味的气体逸出,当溶液恰好澄清时,关闭F,然后往烧杯中加入热水,静止一会,观察到III中试管壁也出现了光亮的银镜,则A是?????????,E中是????????与葡萄糖的混合液(写化学式)。请写出反应管C中所发生反应的方程式:????????????????????????????????。仪器D在此实验中的作用是???????????????????。
⑶若B为浓硫酸,E为苯酚钠溶液,C仍旧不变,A是只含一个碳的一种有机物也能发生银镜反应,实验中同样能观察到C中黑色固体逐渐变红,同时可观察到试管中溶液变浑浊,则A可能是??????????????????????????,然后往烧杯中加入沸水,可观察到试管中的现象是????????????????????????????????????,此实验中浓硫酸的作用是????????????????。写出(1)中A和(3)中A二种物质在浓硫酸存在时所发生的反应方程式:???????????????????????????????????????????????????????????,此反应中浓硫酸的作用是?????????????。
参考答案:(13分)(1)乙醇???? CuO?? CuO+CH3CH
本题解析:略
本题难度:简单
3、实验题 某研究小组探究SO2和Fe(NO3)3溶液的反应。
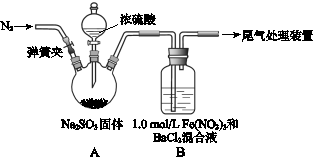
已知: 1.0 mol・L-1的Fe(NO3)3溶液的pH=1,请回答:
(1)装置A中反应的化学方程式是????????。
(2)为排除空气对实验的干扰,滴加浓硫酸之前应进行的操作是????????。
(3)装置B中产生了白色沉淀,其成分是????????,说明SO2具有????????性。
(4)分析B中产生白色沉淀的原因:
观点1:????????_____________________________;
观点2:SO2与Fe3+反应;
观点3:在酸性条件下SO2与NO3-反应;
①若观点2正确,装置B中反应的离子方程式是????????。
②只需将装置B中的 Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验,即可证明观点3是否正确,应选择的试剂是(填序号)????????。
a.0.1 mol・L-1稀硝酸?????????????????????
b.1.5 mol・L-1 Fe(NO3)2溶液
c.6.0 mol・L-1 NaNO3和0.2 mol/L盐酸等体积混合的溶液
参考答案:(12分)
(1)Na2SO3+H2SO4(浓)=Na
本题解析:
试题分析:(1)装置A中的反应是制取SO2,方程式为:Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O。
(2)反应前要充入N2,排除装置A中的空气,反应对实验的干扰。
(3)硝酸具有氧化性,白色沉淀为BaSO4,说明SO2具有还原性。
(4)经过分析,各个观点,得出观点1是SO2和Fe3+、酸性条件下NO3-都反应。
①Fe3+把SO2氧化,离子方程式是SO2+2Fe3++Ba2++2H2O=BaSO4↓+2Fe2++4H+。
②Fe(NO3)3中有Fe3+,a错;NO3-在酸性条件下有氧化性,b错。故选c。2制备 Fe3+、NO3-的氧化性
点评:本题考查的是SO2制备和Fe3+、NO3-的氧化性的相关知识,题目难度较大,要求学生熟悉所实验的内容及原理,能够考查同学们进行分析问题、解决问题的能力。
本题难度:一般
4、实验题 (8分)实验室常用氧化浓盐酸的方法制取氯气,课本中实验装置如下图:
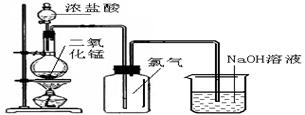
⑴写出制氯气的化学方程式:???????????????????,
⑵甲同学认为该装置制得的氯气不纯,在收集氯气之前补充了下面实验装置,你认为如何连接(用ABCD字母连接):????????????。浓硫酸的作用??????????????????????????,
饱和食盐水的作用是??????????????????????????????。
参考答案:①MnO2 + 4HCl(浓)  本题解析:
本题解析:
试题分析:(1)实验室制氯气的反应方程式为:MnO2 + 4HCl(浓)  MnCl2 + Cl2↑+ 2H2O
MnCl2 + Cl2↑+ 2H2O
(2)实验室制取的氯气含有杂质HCl和水蒸气,应该先除HCl再除水蒸气,除去HCl用饱和食盐水,除去水蒸气用浓硫酸。
点评:本题主要考查学生的基础知识,非常简单。
本题难度:一般
5、实验题 海带中含有丰富的碘元素(以I-形式存在)。实验室中提取碘的流程如下:(已知:Cl2 + 2KI =" 2KCl" + I2)
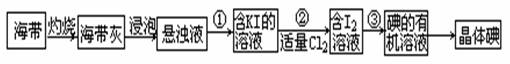
(1)提取碘的流程中:步骤①需要的主要仪器是??????????,步骤③需要的主要仪器是??????????(填序号)
 ?
?
(2)写出步骤②中涉及的有关离子反应方程式???????????????????????????。
(3)提取碘的过程中,可供选择的有机试剂有??????????。
A.四氯化碳
B.醋酸
C.酒精
D.苯
参考答案:(1)? ② (1分)??
本题解析:略
本题难度:简单