��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �±��У����й����ӷ���ʽ���Ȼ�ѧ����ʽ�����ۺ������� [???? ]
���ӷ���ʽ���Ȼ�ѧ����ʽ
����
A.
NaHSO4�����ڣ�=Na++HSO4-
����HSO4-Ӧ����ΪH+��SO42-
B.
HCO3-+H2O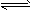 CO32-+H3O+?
CO32-+H3O+?
��ȷ����HCO3-ˮ������ӷ���ʽ
C.
2H2(g)+O2(g)=2H2O(g) ��H=-241.8 kJ/mol
��ȷ��������ȼ����Ϊ-241.8 kJ/mol
D.
H+(aq) +OH-(aq)=H2O(l) ��H=+57.3 kJ/mol
�����кͷ�ӦΪ���ȷ�Ӧ
2��ѡ���� �����Ȼ�ѧ����ʽ��д��ȷ����(����)
A��2SO2��O2 2SO3����H����196.6 kJ��mol��1
2SO3����H����196.6 kJ��mol��1
B��C(s)��O2(g)===CO2(g)����H����393.5 kJ��mol��1
C��H2(g)��Cl2(g)===HCl(g)����H����92.5 kJ��mol��1
D��H��(aq)��OH��(aq)===H2O(l)����H����57.3 kJ
3������� ��1������ͬ����CO��g����H2O��g���ֱ�ͨ�����2L�ĺ����ܱ������У����з�ӦCO��g��+H2O��g��?CO2��g��+H2��g�����õ������������ݣ�
| ʵ���� | �¶ȡ� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min
CO
H2O
H2
CO
1
650
4
2
1.6
2.4
6
2
900
2
1
0.4
1.6
3
��ʵ��1����v��CO2����ʾ�ķ�Ӧ����Ϊ______���ڶ�λС����
�ڸ÷�ӦΪ______������ȡ����ȡ�����Ӧ��
����ʵ��2��ƽ������K��Ҫ��д��������̣����ȡ��λС��
��2����֪�ڳ��³�ѹ�£���2CH3OH��1��+3O2��g��=2CO2��g��+4H2O��1����H=-1451.6kJ/mol
��2CO��g��+O2��g��=2CO2��g����H=-566.0kJ/mol
д���״�����ȫȼ������CO��Һ̬ˮ���Ȼ�ѧ����ʽ______
��3���״���������ȫȼ�յķ�Ӧ�������Ϊȼ�ϵ�أ�װ����ͼ���õ��ͨ��K2CO3��Һ���շ�Ӧ����CO2�����ĵ缫��ӦΪ______��
��4��CaCO3��KSP=2.8��10-9���������CaCl2��Һ��Na2CO3��Һ��ϣ���Na2CO3��Һ��Ũ��Ϊ2��10-4mol/L�������ɳ��������CaCl2��Һ����СŨ��Ϊ______��
4��ѡ���� �����Ȼ�ѧ����ʽ����101kPaʱ����S��s��+O2��g���TSO2��g����H=-297.23kJ/mol����������˵���в���ȷ���� �� ? �� A��S��ȼ����Ϊ297.23?kJ/mol
B���γ�1?mol?SO2�Ļ�ѧ�����ͷŵ����������ڶ���1?mol?S��s����1?mol?O2��g���Ļ�ѧ�������յ�������
C��S��g��+O2��g���TSO2��g���ų�������С��297.23?kJ
D��S��g��+O2��g���TSO2��g���ų�����������297.23?kJ
5��ѡ���� 25�桢101kPa�£�̼������������������ǵ�ȼ����������393.5kJ/mol��285.8kJ/mol��890.3kJ/mol��2800kJ/mol���������Ȼ�ѧ����ʽ��ȷ����[???? ]
A��C(s)+1/2O2(g)==CO(g) ��H��-393.5kJ/mol
B��2H2(g)+O2(g)==2H2O(g) ��H��+571.6kJ/mol
C��CH4(g)+2O2(g)==CO2(g)+2H2O(g) ��H��-890.3kJ/mol
D��1/2C6H12O6(s)+3O2(g)==3CO2(g)+3H2O(l) ��H��-1400kJ/mol
|
��վ�ͷ�QQ: 960335752 - 14613519 - 791315772