微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各组物质中,所含分子数相同的是( )
A.10gH2和10gO2
B.5.6LN2(标准状况)和11gCO2
C.9gH2O和0.6molBr2
D.224mLH2(标准状况)和0.1molN2
参考答案:B
本题解析:只要物质的物质的量相等,则根据 可知,物质的分子数就是相等的。选项A中氢气的物质的量是5mol,氧气的物质的量是10/32mol;B中氨气的物质的量是0.25mol,CO2的物质的量也是0.25mol;C中水的物质的量是0.5mol;D中氢气的物质的量是0.01mol,所以正确的答案选B。
可知,物质的分子数就是相等的。选项A中氢气的物质的量是5mol,氧气的物质的量是10/32mol;B中氨气的物质的量是0.25mol,CO2的物质的量也是0.25mol;C中水的物质的量是0.5mol;D中氢气的物质的量是0.01mol,所以正确的答案选B。
本题难度:一般
2、计算题 (4分)把13 g含有SiO2的CaCO3固体在高温下加热到质量不再改变,冷却后称量为8.6 g则生成的CO2在标准状况下的体积为????????L,原混合物中含SiO2的质量?????????g。
参考答案:(4分)2.24???? 3
本题解析:
试题分析:二氧化硅和碳酸钙再高温下反应生成硅酸钙和CO2,如果碳酸钙过量,则碳酸钙继续分解生成氧化钙和CO2。所以不论再什么情况下,固体减少的质量一定是生成的CO2的质量,即CO2的质量是13g-8.6g=4.4g,物质的量是0.1mol,标准状况下的体积是2.24L。根据碳原子守恒可知,碳酸钙的物质的量是0.1mol,质量是10g,所以二氧化硅的质量是3g。
点评:该题是基础性试题的考查,难度不大。该题的关键是利用好守恒法,有利于培养学生的应试能力,提高学生的学习效率。
本题难度:一般
3、选择题 设NA为阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,1.12LCCl4含有C-Cl键数目为0.2NA
B.标准状况下,2.24L氯气中含有的 Cl数目一定为0.2NA
Cl数目一定为0.2NA
C.常温常压下,4.4gCO2与N2O混合气体中含有的原子总数为0.3NA
D.80mL 10mol・L-1盐酸与足量MnO2加热反应,产生Cl2分子数为0.2NA
参考答案:C
本题解析:
试题分析:A、CCl4为液态,不能用气体摩尔体积计算,错误;B、天然的氯元素有2种同位素,其总量为0.2NA,错误;C、CO2与N2O摩尔质量相同,分子中原子个数相同,故原子个数为4.4÷44×3=0.3mol,正确;D、该反应中盐酸为浓盐酸,随反应进行盐酸浓度降低不再反应,故产生的Cl2分子数小于0.2NA,错误。
本题难度:一般
4、实验题 (9分)实验室欲用NaOH固体配制1.0mol/L的NaOH溶液480mL:
(1)配制时,必须使用到的玻璃仪器有 、 、 、
(2) 使用容量瓶前必须进行的一步操作是_____________________
(3) 要完成本实验该同学应称出NaOH______g
(4)在配制过程中,其他操作都是正确的,下列操作会引起所配溶液浓度偏高的是__________
①称量固体药品时所用的砝码是生锈的
②称量时间过长
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤未冷却到室温就将溶液转移到容量瓶并定容
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度
参考答案:(1)烧杯、玻璃棒、 500mL容量瓶、胶头滴管
本题解析:
试题分析:(1)配制时需要的仪器主要有烧杯、玻璃棒、500mL容量瓶、胶头滴管。
(2)容量瓶带盖,所以使用前必须捡漏。
(3)因为没有480mL的容量瓶,所以配制过程中需要500mL容量瓶,溶质质量也要按照500mL容量瓶来计算,所以m(NaOH)=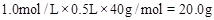 。
。
(4)根据c= 可知,砝码生锈称量的固体质量比正常值高,所以偏高,称量时间过长NaOH会变质,所以偏低,容量瓶不干燥,溶质质量和溶液体积都无影响,所以无影响,定容时俯视刻度,溶液的体积比正常值小,所以偏高,为冷却就定容,溶液冷却后溶液的体积会缩小,所以偏高,摇匀后又加水,溶液的体积比正常值大,所以偏低。因此偏高的是①④⑤。
可知,砝码生锈称量的固体质量比正常值高,所以偏高,称量时间过长NaOH会变质,所以偏低,容量瓶不干燥,溶质质量和溶液体积都无影响,所以无影响,定容时俯视刻度,溶液的体积比正常值小,所以偏高,为冷却就定容,溶液冷却后溶液的体积会缩小,所以偏高,摇匀后又加水,溶液的体积比正常值大,所以偏低。因此偏高的是①④⑤。
考点:物质的量浓度配制
点评:
本题难度:一般
5、选择题 某500mL溶液中含有0.1 mol Fe2+、0.2 mol Fe3+,加入0.2 mol铁粉,待Fe3+完全还原后,溶液中Fe2+的物质的量浓度为(假设反应前后体积不变)[???? ]
A.0.4mol・L-1
B.0.6mol・L-1
C.0.8mol・L-1
D.1.0mol・L-1
参考答案:C
本题解析:
本题难度:简单