微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 浓度为0.01mol・L-1的HCl溶液10mL,加水稀释到20mL,取稀释后的溶液1mL,这1mL溶液中的C(H+) 为 ( )
A.0.0005mol/L
B.0.001mol/L
C.0.002mol/L
D.0.005mol/L
参考答案:D
本题解析:稀释过程中溶质的物质的量不变,有0.01×10=c×20,得c=0.005mol/L,从该溶液中取出1mL浓度不变。答案选D。
本题难度:简单
2、选择题 配制450毫升1mol/L的食盐溶液需选择的容量瓶是( )
A 100ml B 500ml C 450ml D50ml
参考答案:B
本题解析:
正确答案:B
没有450毫升规格的容量瓶,一次配成450毫升溶液,只能选500毫升的容量瓶
本题难度:简单
3、选择题 0.1mol?L-1BaCl2溶液100mL,和0.08mol?L-1AgNO3溶液1000mL充分混合后又加入0.06mol?L-1ZnSO41000mL,最后溶液中浓度最大的离子是( )
A.Cl-
B.Zn2+
C.Ag+
D.NO3-
参考答案:0.1mol?L-1BaCl2溶液100mL中n(Ba2+)
本题解析:
本题难度:简单
4、选择题 硫酸镁和硫酸铝溶液等体积混合后,铝离子浓度为0.2mol・L-1,硫酸根离子的浓度为0.4mol・L-1,则混合液中镁离子的浓度为 ( )
A.0.1mol・L-1
B.0.15mol・L-1
C.0.2mol・L-1
D.0.3mol・L-1
参考答案:A
本题解析:
试题分析:根据溶液的电中性可知:电荷守恒,即3c(Al3)+2c(Mg2+)=2c(SO42―),所以溶液中2c(Mg2+)=(2×0.4mol/L-3×0.2mol/L)=0.2mol/L,c(Mg2+)= 0.1mol・L-1,答案选A。
考点:考查溶液中离子浓度大小的有关计算。
本题难度:一般
5、选择题 将5mol/L的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO3-的物质的量浓度是
A.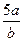 mol/L
mol/L
B.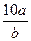 mol/L
mol/L
C.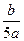 mol/
mol/ L
L
D.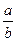 mol/L
mol/L
参考答案:B
本题解析:略
本题难度:一般