微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (7分)金属钒(V)在材料科学上有重要作用,被称为“合金的维生素”。以下是测定矿石中钒的含量的两个反应:
(1)用稀硫酸溶解五氧化二钒,得到(VO2)2SO4溶液。写出该反应的化学方程式
____________________________________________________________;
该反应______(选填“是”或“不是”)氧化还原反应。
(2)用已知浓度的硫酸酸化的H2C2O4溶液,滴定(VO2)2SO4溶液,完成下列离子方程式,方框内填数字,短线上填写物质的化学式或离子符号。
VO2+ + H2C2O4 + ______ → VO2+ + CO2 + ______
(3)当收集到标准状况下气体112毫升时,电子转移的数目为
(4)甲同学提出:上述反应能否用盐酸酸化?乙同学认为:要回答这个问题还得知道
A.VO2+ 和HCl氧化性相对强弱 B.VO2+ 和Cl2氧化来源:91考试网 www.91exAm.org性相对强弱 C.上述均不正确.
参考答案:(1)V2O5+H2SO4=(VO2)2 SO4+H2O&#
本题解析:
试题分析:(1)用稀硫酸溶解五氧化二钒,得到(VO2)2SO4溶液,化学方程式为V2O5+H2SO4=(VO2)2 SO4+H2O;该反应中的各元素的化合价在反应前后未发生变化,所以不是氧化还原反应;
(2)VO2+V的化合价是+5价,产物中V的化合价是+4价,H2C2O4中C的化合价是+3价,二氧化碳中C的化合价是+4价,所以C的化合价整体升高2价,根据氧化还原反应中得失电子守恒,VO2+、VO2+的系数是2,H2C2O4,的系数是1,二氧化碳的系数是2,根据电荷守恒,反应物中的电荷小于产物中的电荷数,所以反应物中的空白应是H+,产物中的空白应是H2O,H+的系数是2,则水的系数是2;
(3)标准状况下气体112毫升,物质的量是0.005mol,即生成0.005mol的二氧化碳,转移电子的物质的量是0.005mol,电子转移的数目为0.005NA
(4)若用盐酸酸化,则盐酸中的氯离子有还原性,所以能否用盐酸酸化,还需知道VO2+ 和Cl2氧化性相对强弱或VO2+与Cl-的还原性的相对强弱,若VO2+ 氧化性强,则不能用盐酸酸化,否则会生成氯气,不能氧化草酸,答案选B。
考点:考查化学方程式的书写,氧化还原反应的判断及配平、计算、氧化还原反应规律的应用
本题难度:一般
2、填空题 (10分)雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
(1) As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。写出此反应的化学方程式?????????????????。
(2)上述反应中的氧化剂是?????????????,氧化产物是??? ??????????。
??????????。
(3) As2S3和HNO3有如下反应:As2S3+ 10HNO3=2H3AsO4+ 3S+10NO2↑+ 2H2O
若生成1mol H3AsO4,则反应中转移电子的物质的量为???????。
(4)在3Cu + 8HNO3= 3Cu(NO3)2 + 2NO↑+4H2O的反应中,有6.4g铜被氧化,参加反应的HNO3的质量是____________g,被还原的HNO3的质量是__________g。
(5)在一定条件下,P bO2与Cr3+反应,产物是Cr2O72-和Pb2+,则生成1mol C
bO2与Cr3+反应,产物是Cr2O72-和Pb2+,则生成1mol C r2O72-
r2O72-
反应所需PbO2的物质的量为__________ ____。
____。
参考答案:(1)2As2S3+2SnCl2 本题解析:略
本题解析:略
本题难度:一般
3、选择题 将0.39g锌粉加入到20.0 mL的0.200 mol・L-1 MO2+溶液中,恰好完全反应,则还原产物可能是
A.M+
B.M2+
C.M3+
D.MO42-
参考答案:B
本题解析:
试题解析:0.39g锌粉完全反应转移的电子是0.012mol??, MO2+中M的化合价是+5,设还原产物中的化合价是x,则有 0.004×(5-x)=0.012,解得x=2;B正确。
本题难度:简单
4、填空题 哈尔滨市场销售的某种食用精制盐包装袋上有如下说明
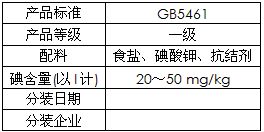
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处):
___KIO3+___KI+___H2SO4 =___K2SO4+___I2+___H2O
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应的离子方程式是_______________________。
②某学生设计回收四氯化碳的操作步骤为:
a.将碘的四氯化碳溶液置于分液漏斗中;
b.加入适量Na2SO3稀溶液;
c.分离出下层液体。
以上设计中遗漏的操作及在上述步骤中的位置是__________________________。
(3)已知:I2+2S2O32-== 2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取wg食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉溶液为指示剂,逐滴加入物质的量浓度为2.0×10-3mol/L的Na2S2O3溶液10.0 mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是___________________。
②b中反应所产生的I2的物质的量是____________mol。
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示) _______________mg/kg。
参考答案:(1)1、5、3、3、3、3
(2)①I2+SO32-
本题解析:
本题难度:一般
5、填空题 交警常用“司机饮酒检测仪”检查司机是否酒后驾车,其原理是硫酸酸化的重铬酸盐(Cr2O72-橙红色)和乙醇反应生成铬盐(Cr3+绿色)和乙酸等。重铬酸钠(Na2Cr2O7)在工业中有很广泛的应用,常用来制备金属铬。方法如下:
将铬铁矿[主要成分Fe(CrO2)2]与纯碱、氧气高温焙烧,除杂、酸化,得到重铬酸钠,碳和重铬酸钠在高温下反应生成Cr2O3、Na2CO3和CO,Cr2O3再经铝热法还原,即可制得金属铬。请回答:
(1)硫酸酸化的K2Cr2O7和乙醇反应的化学方程式是 。
(2)写出碳和重铬酸钠高温反应的化学方程式 。
Cr2O3经铝热法还原制得金属铬的化学方程式是 。
(3)硫酸酸化的Na2Cr2O7和FeSO4反应,生成Cr3+等,该反应的离子方程式是 。
(4)某Na2Cr2O7样品2.00g恰好和4.56gFeSO4完全反应,该样品的纯度为 。
参考答案:⑴2K2Cr2O7 + 3CH3CH2OH + 8H2SO4
本题解析:略
本题难度:简单