微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知AgCl的溶解平衡:AgCl(s)?Ag+(aq)+Cl-(aq)下列说法不正确的是( )
A.除去溶液中Ag+加盐酸盐比硫酸盐好
B.加入H20,溶解平衡不移动
C.用NaCl溶液代替蒸馏水洗涤AgCl,可以减少沉淀损失
D.反应2AgCl+Na2S═Ag2S+2NaCl说明溶解度:AgCl>Ag2S
参考答案:A、氯化银溶解度小于硫酸银,除去溶液中Ag+加盐酸盐比硫酸盐
本题解析:
本题难度:一般
2、选择题 以MnO2为原料制得的MnCl2溶液中常含有Cu2+、Pb2+、Cd2+等金属离子,通过添加过量难溶电解质
MnS,可使这些金属离子形成硫化物沉淀,经过滤除去包括MnS在内的沉淀,再经蒸发、结晶,可得纯净的MnCl2,根据上述实验事实可推知MnS具有的相关性质是 [???? ]
A.具有吸附性
B.溶解度与CuS、PbS、CdS等相同
C.溶解度大于CuS、PbS、CdS
D.溶解度小于CuS、PbS、CdS
参考答案:C
本题解析:
本题难度:一般
3、选择题 下列说法中合理的是 [???? ]
A.在Na2S溶液中加入AgCl固体,溶液中c(S2-)会下降
B.常温下,AgCl在物质的量浓度相同的CaCl2溶液和NaCl溶液中的溶解度相同
C.向0.1 mol/L的ZnCl2溶液中通入足量的H2S气体,最终得不到沉淀是因为c(S2-)·c(Zn2+)<Ksp(ZnS)
D.25℃时,Ksp[Mg(OH)2]=5.61×10-12、Ksp(MgF2)=7. 42×10-11;则向Mg(OH)2悬浊液中加入NaF溶液后,Mg(OH)2不可能转化为MgF2
参考答案:A
本题解析:
本题难度:一般
4、选择题 在BaSO3(s)?Ba2+(aq)+SO32- (aq)平衡体系中,下列措施可使沉淀量减少的是( )
A.加入K2SO3(s)
B.加入稀HNO3
C.加入稀盐酸
D.加入K2SO4(s)
参考答案:A、加入K2SO3(s),K2SO3电离产生SO32-,SO
本题解析:
本题难度:简单
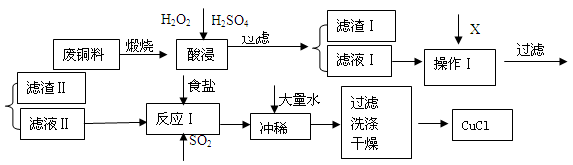
5、简答题 (14分) CuCl是有机合成的重要催化剂,并用于颜料、防腐等工业。工业上由废铜料(含Fe、Al及其化合物、SiO2杂质),生产CuCl的工艺流程如下:
物质
| 开始沉淀
| 沉淀完全
|
Fe(OH)3
| 2.7
| 3.7
|
Cu(OH)2
| 5.6
| 6.7
|
Al(OH)3
| 3.8
| 4.7
?
已知:CuCl溶于NaCl的浓溶液可生成CuCl2-,CuCl2-的溶液用水稀释后可生成CuCl沉淀。
(1)煅烧的主要目的是:??????????????????????????????????????。
(2)操作Ⅰ为调节溶液的PH值,范围为???????,加入的物质X可以是(????)
A、CuO??? B、Cu(OH)2????? C、NaOH 溶液???? D、CaCO3
(3)滤渣Ⅱ的主要成分是?????????。
(4)往滤液Ⅱ中加入食盐并通入SO2可生成CuCl2-,请写出反应的离子方程式:???????????????????。??
(5)在反应Ⅰ中,温度控制在70~80℃并使用浓NaCl溶液,主要目的是:???????????????。
(6)常温下,已知CuOH的KSP为1.0×10-14,则Cu++H2O  CuOH + H+的平衡常数为:??????????。 CuOH + H+的平衡常数为:??????????。
参考答案:(1)使铜转化为可溶于酸的氧化物 (2)4.7≤PH<
本题解析:
试题分析:(1)煅烧的主要目的是使铜转化为可溶于酸的氧化物。(2)操作Ⅰ为调节溶液的PH值,要想溶液中加入的物质消耗H+,同时不引入新的杂质离子,对后边的形成CuCl沉淀有利的物质,应该是CuO、Cu(OH)2、NaOH 溶液。因此选项为A、B、C。调整溶液的pH的范围应该是使杂质离子形成沉淀除去而Cu2+留在溶液中,根据表格提供的数据,应该在4.7~5.6。(3)此时产生的滤渣Ⅱ的主要成分是Fe(OH)3?和Al(OH)3;(4)往滤液Ⅱ中加入食盐并通入SO2发生氧化反应反应,可生成CuCl2-
本题难度:一般
|