��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��1�� 8gҺ̬��CH3OH����������ȫȼ�գ����ɶ�����̼�����Һ̬ˮʱ�ͷų�Q kJ����������д��Һ̬CH3OHȼ���ȵ��Ȼ�ѧ����ʽ ��
��2���ڻ�ѧ��Ӧ�����У��ƻ��ɻ�ѧ����Ҫ�����������γ��»�ѧ���ֻ��ͷ�������
��ѧ��
| H��H
| N��H
| N��N
|
����/kJ·mol��1
| 436
| 391
| 945
��֪��ӦN2��3H2=2NH3����H��a KJ/mol��
�Ը��ݱ������м������ݼ���a����ֵΪ�� ��
��3����֪��C(s��ʯī)��O2(g)=CO2(g) ��H1����393.5 kJ/mol
2H2(g)��O2(g)=2H2O(l) ��H2����571.6 kJ/mol
2C2H2(g)��5O2(g)=4CO2(g)��2H2O(l) ��H3����2599 kJ/mol
���ݸ�˹���ɣ���C(s��ʯī)��H2(g)����1 mol C2H2(g)��Ӧ���Ȼ�ѧ����ʽ��
��
�ο��𰸣�.��1��CH3OH(l)+3/2 O2(g)="=" CO2
���������
�����������1�� ȼ������1 mol��ȼ����ȫȼ�������ȶ��������ͷŵ�������8g CH3OHȼ�շ���Q kJ����1 molCH3OH��ȫȼ�շ���4Q kJ.����CH3OH(l)+ O2(g)="=" CO2(g)+2H2O(l) ��H����4QKJ/mol��
��2�� ��H=��Ӧ��ļ����ܺ�-������ļ����ܺ�=��945+3��436��kJ/mol -2��3��391 kJ/mol ="-93" kJ/mol����a=-93
��3�� ��C(s��ʯī)��O2(g)=CO2(g) ��H1����393.5 kJ/mol ��
2H2(g)��O2(g)=2H2O(l) ��H2����571.6 kJ/mol ��
2C2H2(g)��5O2(g)=4CO2(g)��2H2O(l) ��H3����2599 kJ/mol ��
�� (�١�4+ ��-��)/2��
2C(s,ʯī)+H2(g)=C2H2(g)  KJ/mol KJ/mol
���㣺��˹���ɵ�Ӧ�ú��Ȼ�ѧ����ʽ����д
�����Ѷȣ�һ��
2��ѡ���� ��֪��2H2(g) +O2(g) �� 2H2O(g) ��H =��483.6 kJ/mol
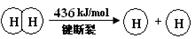
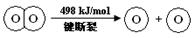
����˵������ȷ����
A���÷�Ӧԭ���������������ȼ�ϵ��
B���ƻ�1 mol H��O ����Ҫ��������463.4 kJ
C��H2O(g)��H2(g) + 1/2O2(g) ��H = +241.8 kJ/mol
D��H2(g) �е�H��H ���� H2O(g) �е�H��O ���ι�
�ο��𰸣�D
���������
�������:A���÷�ӦΪ������ԭ��Ӧ�����Ƿ��ȷ�Ӧ��������Ƴ�ԭ��أ�A��ȷ����Ӧ��=��Ӧ����ܼ���-��������ܼ���=436x2+498-4x=-483.6��x=241.8����B��ȷ��2H2(g) +O2(g) �� 2H2O(g)����H =��483.6 kJ/mol �����淴Ӧ��������Ϊ+483.6kJ/mol��1molˮ�ֽ���������Ϊ241.8 kJ/mol��C��ȷ������Խ��Խ�ȶ�����H2(g) �е�H��H ������ H2O(g) �е�H��O ���ι̣�D����ѡD
���㣺��Ӧ����ԭ���ԭ��
�����Ѷȣ�һ��
3��ѡ���� ���������У���ȷ���ǣ������� A������ı�ȼ����Ϊ890.3?kJ?mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4��g��+2O2��g���TCO2��g��+2H2O��g����H=-890.3?kJ?mol-1
B��500�桢30?MPa�£���0.5?mol?N2��1.5?mol?H2�����ܱյ������г�ַ�Ӧ����NH3��g��������19.3?kJ�����Ȼ�ѧ����ʽΪ��
N2��g��+3H2��g�� 2NH3��g����H=-38.6?kJ?mol-1 2NH3��g����H=-38.6?kJ?mol-1
C����ͬ�����£�2mol��ԭ�������е�����С��1mol����������е�����
D�������£���ӦC��s��+CO2��g���T2CO��g�������Է����У���÷�Ӧ�ġ�H��0
�ο��𰸣�D
���������
�����Ѷȣ���
4������� ��15�֣�
��1����֪��
�״���ϩ����Ӧ�٣�2CH3OH(g)��C2H4 (g)��2H2O(g)?��H1����29��0 KJ��mol��1
�״���ˮ��Ӧ�ڣ�2CH3OH(g)��CH3OCH3(g)��H2O(g)?��H2����24��0 KJ��mol��1
�Ҵ��칹����Ӧ�ۣ�CH3CH2OH(g)��CH3OCH3(g))?��H3��+50��8 KJ��mol��1
����ϩ����ֱ��ˮ�Ϸ�ӦC2H4 (g)��H2O(g)��C2H5OH(g)��?��H�� KJ��mol��1
��2���ھ��Ʊ���ʳ��ˮ�м���̼����刺��Ʊ�С�մ�NaHCO3��������ȡ�Ȼ����Ϊ���ϻ��һ���ᴿΪ��ҵ�Ȼ�李�
��д�������Ʊ�С�մ�Ļ�ѧ����ʽ��__________________________________��
���˳�С�մ��ĸҺ��ȡ�Ȼ�������ַ�������ͨ�백����ȴ����ʳ�Σ����ˣ���ͨ������ȴ����ʳ�Σ����ˡ����з������������Ȼ�淋Ĵ��ȸ��ߣ���ԭ���� ������������ŵ�������Һ���� ��
��3��Ǧ���仯������������أ������豸��X���߷������ϵȡ�PbO2����PbO�����������Һ��Ӧ�Ƶã���Ӧ�����ӷ���ʽΪ ��PbO2Ҳ����ͨ��ʯīΪ�缫��Pb(NO3)2��Cu(NO3)2�Ļ����ҺΪ���Һ�����ȡ�����������ĵ缫��Ӧʽ �����Һ�м���Cu(NO3)2��ԭ���� ��
�ο��𰸣���14�֣� ��1��-45.8
��2�� ��NH4HCO3
���������
�����������1�����ݸ�˹���ɣ���-��-�ۿɵ������Ȼ�ѧ����ʽ������ϩ����ֱ��ˮ�Ϸ�ӦC2H4 (g)��H2O(g)��C2H5OH(g)��?��H����-��-��=����24��0+29-50.8��kJ/mol=-45.8kJ/mol��
��2���ٸ��������ܽ�ȵIJ�ͬ���Ȼ��Ƶ��ܽ�ȴ���̼�����Ƶ��ܽ�ȣ������͵��Ȼ�����Һ�м���̼����泥�������̼�����Ƴ������Ȼ�泥���ѧ����ʽ��NH4HCO3+NaCl��NaHCO3��+NH4Cl��
��I��II�����������Ƿ�ͨ�백������ͨ�백�������Ȼ�淋�Ũ��������ʳ�κ����������������Ȼ�淋�������������I���˺����Һ�к��а��������Բ���ѭ��ʹ�ã�����II���˺����ҺΪ�Ȼ��ƣ���ֱ��ѭ��ʹ�ã�
��3��PbO��������Ʒ�Ӧ����PbO2��PbԪ�صĻ��ϼ����ߣ���ClԪ�صĻ��ϼ۽��ͣ����Դ���������ӱ���ԭΪ�����ӣ����ӷ���ʽ��PbO+ClO-= PbO2+Cl-�����ʱ����������������Ӧ����Ϊ�õ��ؿ���ȡPbO2������������Pb2+ʧȥ������ˮ�������PbO2���缫��Ӧʽ��Pb2++2H2O-2e- = PbO2��+ 4H+��������������ͭ���������������ӷŵ磬���������ŵ����Pb2+������Pb�����������ϵõ�PbO2���������٣�Pb2+�������ʽ��͡�
���㣺�����˹���ɵ�Ӧ�ã���ʵ�鷽���ķ������绯ѧ��Ӧԭ����Ӧ��
�����Ѷȣ�����
5������� ��֪��
N2H4(g)+O2=N2(g)+2H2O(g) ��H��-543kJ/mol
1/2H2(g)+1/2F2(g)=HF(g) ��H��-269kJ/mol? ��H��-242kJ/mol
��д��N2H4��F2��Ӧ���Ȼ�ѧ����ʽ��__________________________________________ ��
�ο��𰸣�![]() ��������� ���������
�����Ѷȣ�һ��
|