微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 相同体积的氯化钠、氯化镁、氯化铝溶液分别与过量的硝酸银溶液反应,所生成的沉淀物质的量相同,则原氯化钠、氯化镁、氯化铝溶液的物质的量浓度之比为
A.6 :3 :2
B.3 :2 :1
C.6 :3 :1
D.1 :2 :3
参考答案:A
本题解析:
试题分析:生成的沉淀即氯化银物质的量相等,说明氯化钠、氯化镁、氯化铝中Cl?物质的量相等,设Cl?物质的量为nmol,则氯化钠的物质的量为nmol,氯化镁的物质的量为1/2nmol,氯化铝的物质的量为1/3nmol,三种溶液体积相同,所以原氯化钠、氯化镁、氯化铝溶液的物质的量浓度之比为n:1/2n:1/3n=6:3:2,故A项正确。
考点:本题考查化学方程式及物质的量浓度的计算。
本题难度:一般
2、填空题 (8分)
① 44.8L某气体在标准状况下的质量为142g,该气体的摩尔质量为_________;
② N2在标准状况下的密度为__________g/L;
③在 mol AL2(SO4)3中含0.3molSO42―,其中含Al3+ 个。
参考答案:(每空2分,共8分)
①71g/mol &#
本题解析:考查物质的量的简单计算
①M=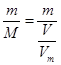 =
=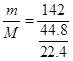 =71g/mol
=71g/mol
②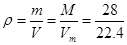 =1.25g/L
=1.25g/L
③由化学式可知道,在0.1mol AL2(SO4)3中含0.3molSO42―,其中含有Al3+0.2mol,即0.2NA个
本题难度:一般
3、选择题 NA表示阿伏加德罗常数,下列判断正确的是
A.含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol・L-1
B.100mL Imol・L-1AlCl3溶液中含的阳离子数大于0.1NA
C.标准状况下,22.4L二氯甲烷的分子数为NA
D.含0.2mol H2SO4的浓硫酸与足量的铜反应,生成的SO2的分子数为0.1NA
参考答案:B
本题解析:略
本题难度:一般
4、填空题 (18分)
(1)实验室有如下仪器:①试管 ②烧杯 ③量筒 ④蒸发皿 ⑤坩埚 ⑥温度计
⑦蒸馏烧瓶,其中可以直接加热的玻璃仪器有________________(填序号)
(2)4.5g水与 g磷酸(H3PO4)所含的分子数相等,它们所含的氧原子数之比是 ,其中氢原子数之比是 。
(3)3.01×1023个OH―的物质的量为 mol,含有电子的物质的量为 mol,这些OH―和 g Na+含有的电子数相同。
(4) 将4gNaOH固体溶于水配成250mL溶液,此溶液中NaOH的物质的量浓度为______mol/L。取出10mL此溶液,其中含有NaOH g。将取出的溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度为______mol/L。
参考答案:23. (1)① ④ (2)24.5
本题解析:
试题分析:(1)实验室中一些仪器可以直接加热,有些需垫石棉网,有些根本就不能被加热.:①试管能直接加热,②烧杯不能直接加热,需要垫石棉网,③量筒是用来量取液体的,不能直接加热,④蒸发皿可以直接加热,⑤坩埚能直接加热,⑥温度计用来测量温度,不能直接加热,⑦蒸馏烧瓶不能直接加热,需要垫石棉网,选择① ④;(2)(3)4.5g水的物质的量n=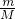 =
=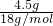 =0.25mol,0.25mol硫酸的质量m=nM=0.25mol×98g/mol=24.5g,0.25mol的水中含有氧原子为0.25mol,0.25mol的磷酸中含有氧原子为1mol,所以氧原子数之比是1:4 ,0.25mol的水中含有氢原子为0.5mol,0.25mol的磷酸中含有氢原子为0.75mol,所以氢原子数之比是2:3,故答案为:24.5g;1:4;2:3.(3)3.01×1023个OH-的物质的量为
=0.25mol,0.25mol硫酸的质量m=nM=0.25mol×98g/mol=24.5g,0.25mol的水中含有氧原子为0.25mol,0.25mol的磷酸中含有氧原子为1mol,所以氧原子数之比是1:4 ,0.25mol的水中含有氢原子为0.5mol,0.25mol的磷酸中含有氢原子为0.75mol,所以氢原子数之比是2:3,故答案为:24.5g;1:4;2:3.(3)3.01×1023个OH-的物质的量为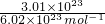 =0.5mol,OH-是10e微粒,含有电子的物质的量为5mol,Na+的核外电子数为与OH-的核外电子数相同,0.5mol Na+的质量为11.5克。(4)n(NaOH)=4/40=0.1mol,则c(A)=0.1/0.25=0.4mol/L;取出10mL,浓度相同,NaOH的质量为:4Х10/250=0.16克。溶液稀释前后溶质的物质的量不变,则c(后)=10Х0.4/100=0.04moL/L。
=0.5mol,OH-是10e微粒,含有电子的物质的量为5mol,Na+的核外电子数为与OH-的核外电子数相同,0.5mol Na+的质量为11.5克。(4)n(NaOH)=4/40=0.1mol,则c(A)=0.1/0.25=0.4mol/L;取出10mL,浓度相同,NaOH的质量为:4Х10/250=0.16克。溶液稀释前后溶质的物质的量不变,则c(后)=10Х0.4/100=0.04moL/L。
考点:考查仪器的使用,物质的量的计算,物质的量浓度的计算等知识。
本题难度:一般
5、选择题 NA为阿伏加德罗常数,下列叙述正确的是(??????)
A.16 g氧气和16 g臭氧所含的原子数均为NA
B.常温常压下,11.2L氯气所含的原子数目为NA
C.2.3g钠由原子变成离子,失去的电子数为1.1NA
D.28g N2中所含的质子数目为7NA
参考答案:A
本题解析:氧气和臭氧都是氧元素形成的不同单质,所以A中氧原子的物质的量是相同的,A正确;常温常压下,11.2L氯气不是0.5mol,B不正确;C不正确,2.3g钠是0.1mol,舍去0.1mol电子;氮元素的质子数是7,28g氮气是1mol,所以含有的质子数是14mol,D不正确,答案选A。
本题难度:一般