��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1�������� �Լ�����FeSO4��Һ�м���NaOH��Һ������д���йط�Ӧ�Ļ�ѧ����ʽ��
�ο��𰸣�������ɫ��״������Ȼ��Ѹ�ٱ�ɻ���ɫ�����ձ�Ϊ���ɫ������<
��������������������ΪB��Fe(OH)2���ױ������� Fe(OH)3��Ҫ��ס��������ɫ�仯�����ǣ�������ɫ��״������Ȼ��Ѹ�ٱ�ɻ���ɫ�����ձ�Ϊ���ɫ������
FeSO4+2NaOH===Fe(OH)2��+Na2SO4??????? 4Fe(OH)2+O2+2H2O===4Fe(OH)3
ѧ��ָ����Ϊ�˸��õؿ����Fe(OH)2��ɫ״̬����ʵ��ʱ����FeSO4��Һ��NaOH��Һ�������ƣ������俪ˮ���ƣ��ɼ���O2����������FeSO4��Һ�м�������ֹFe2+������Fe3+�����ó��Ľ�ͷ�ι���ȡNaOH��
�����Ѷȣ���
2��ѡ���� ��������(Na2FeO4)��������ǿ�ڸ�����غͳ�������һ�ָ�Ч��ܾ�ˮ��������������ڸ������ƾ�ˮ���õ���������ȷ����
A? Na2FeO4�ھ�ˮ��������ת�����������
B? Na2FeO4��ɱ������
C? Na2FeO4�ܳ�ȥˮ�е�����Ȼ�ԭ����������
D? Na2FeO4������ˮ�е���ɫ�������
�ο��𰸣�D
�����������
�����Ѷȣ���
3������� A�������ʽṹ�����ʡ�ģ�飨12�֣�
��ï����(C5H5)2 Fe������һ�����������Ӻ�2������ϩ�������ӹ��ɣ����ķ��ֿ���˵���л������������о��о�����̱�������¼����������˽����л��������о��������ٽ��˽����л���ѧ�ķ�չ����ï�������û�ԭ�����뻷���ϩ�ڵ�����Χ�з�����Ӧ���Ƶã�
2C5H6��Fe(��ԭ����)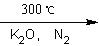 (C5H5)2 Fe��H2��
(C5H5)2 Fe��H2��
��ش��������⣺
��1��д�����������ӵĻ�̬�����Ų�ʽ��???????????????????????????????????��
��2����ï�����۵���173�棨��100��ʱ��ʼ���������е���249�棬������ˮ�������ڱ������ѵȷǼ����ܼ����ݴ˿��ƶ϶�ï������Ϊ????????????���壬�ɴ˿ɽ�һ����֪���ڶ�ï���ṹ�У�C5H5����Fe2+֮���γɵĻ�ѧ��������????????????????��
��3�������ϩ�ĽṹʽΪ��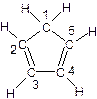 ��ͼ�����ֽ�����̼ԭ�ӱ�ţ�������5��̼ԭ���в�ȡsp3�ӻ�����???????����д��ţ���
��ͼ�����ֽ�����̼ԭ�ӱ�ţ�������5��̼ԭ���в�ȡsp3�ӻ�����???????����д��ţ��� �ǻ�ï��ϩ��һ��ͬ���칹�壬������ӽṹ�д���ͬһƽ���ϵ�ԭ�Ӹ��������?????����
�ǻ�ï��ϩ��һ��ͬ���칹�壬������ӽṹ�д���ͬһƽ���ϵ�ԭ�Ӹ��������?????����
��4��ԭ����Ŀ�͵�����������۵�����������ͬ������Ϊ�ȵ����壬�ȵ�����������ƵĽṹ��������N2���ӻ�Ϊ�ȵ�����Ķ�����������????????���ѧʽ���������ʽ��?????????????????????????��
B����ʵ�黯ѧ��ģ�飨12�֣�
��12�֣�ij����С��Ϊ�˲ⶨij�Ȼ��ȣ�SrCl2����Ʒ�Ĵ��ȣ��ڽ�ʦָ������������·�����
��ȡ1.0g��Ʒ�ܽ�������ˮ�У������м��뺬AgNO32.38g��AgNO3��Һ����Һ�г�Cl�D�⣬����������Ag+��Ӧ���ɳ��������ӣ���Cl�D����ȫ��������Ȼ���ú�Fe3+����Һ��ָʾ������NH4SCN����Һ�ζ�ʣ���AgNO3��ʹʣ���Ag+��AgSCN��ɫ��������ʽ�������Բⶨ�Ȼ�����Ʒ�Ĵ��ȡ���ش��������⣺
��1���ζ���Ӧ�ﵽ�յ�������ǣ�?????????????????????????????????????????��
��2��ʵʩ�ζ�����Һ�Գ�?????????????��ѡ����ԡ��������ԡ����ԡ���Ϊ�ѣ�����??????????????????���ѧʽ���Լ��ɴ���һĿ�ġ�
��3�����յ㵽��֮ǰ�ĵζ������У����ֳ����������������Ag+���費�Ͼ���ҡ����ƿ�������ʹn (Cl��)�IJⶨ���??????????��ѡ�ƫ�ߡ�����ƫ�͡�����Ӱ�족����
��4�������յ�����������ҡ����ƿ������ʱ���þ���ҡ�����Լ�����������������ʹn (Cl��)�ⶨֵƫ�ͣ���˵�����ߵ��ܽ�ȣ�AgCl???????AgSCN
���������������
��5������Fe3+����Һ��ָʾ������NH4SCN����Һ�ζ�ʣ���AgNO3ʱ����ȥ����Ũ�ȵ�NH4SCN��Һ20.0mL����ԭ�Ȼ�����Ʒ�Ĵ���Ϊ?????????????????��
�ο��𰸣�A�������ʽṹ�����ʡ�ģ�飨12�֣�
��1��1s22s
���������A ��ï�����۵���173�棨��100��ʱ��ʼ���������е���249�棬������ˮ�������ڱ������ѵȷǼ����ܼ����ɼ���ï���۷е�;��з��Ӿ����ص㡣Fe2+�ṩ�չ����C5H5���ṩ�µ��Ӷԣ��Ӷ��γ���λ����
�����Ѷȣ�һ��
4��ʵ���� ij����С�����������ͼ��ʾ��ʵ��װ�ý���ʵ�顣�ش��������⣺
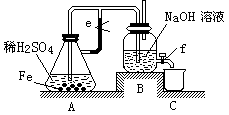
�� ��ʼʵ��ʱ���ɼ�e�Ǵģ�A�з�����Ӧ�����ӷ���ʽΪ��???????????????????��
B�п��Թ۲쵽��������????????????????????????????????????????????��
�� �����Ӻ���ϵ��ɼ�e��B�п��Թ۲쵽��������??????????????????????????????��
�� �����������f�ŵ�2��3Һ�壬B�пɹ۲쵽��������??????????????????????????��
�йط�Ӧ�Ļ�ѧ����ʽ��??????????????????????????????????????????��
�ο��𰸣���1�� Fe+2H+==Fe2++H2����������ð��?��2��
���������
�����������1������ϡ���ᷴӦ����������������������Ӧ�����ӷ���ʽ��Fe+2H+==Fe2++H2��������������ˮ������B�п��Թ۲쵽��������������ð����
��2������A�еķ�Ӧ��û��ֹͣ�������ɵ���������������ˮ���������ŷ�Ӧ�Ľ��У�A�е�ѹǿ������Һѹ��B�У��Ӷ�����������������ɫ������
��3�������������f�ŵ�2��3Һ�壬�����������B�С��������������ּ��ױ�����������ʵ�������ǰ�ɫ�����ȱ�ɻ���ɫ������ɺ��ɫ��������Ӧ�Ļ�ѧ����ʽ�� 4Fe(OH)2+O2+2H2O==4
�����Ѷȣ�һ��
5��ѡ���� ����ƬͶ��������Һ�У�һ��ʱ���ȡ���������������Ƭ�������ӵ���
A��ϡ����
B������п��Һ
C������ͭ��Һ
D���Ҵ���Һ
�ο��𰸣�C
���������
���������A������ϡ���ᷴӦ����Ƭ������С��B�в��䡣 C���û���ͭ������Ƭ�ϣ��������ӡ�D��Ƭ�������仯��
�����Ѷȣ�һ��