2.6
�ش��������⣺
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK��????????????????????????????????��
��2���÷�ӦΪ???????????��Ӧ��ѡ�����ȡ����ȣ���
��3�����жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬��������???????????????��
a��������ѹǿ����???????????????? b�����������c��CO������
c��������H2�������棨H2O��????????? d��c��CO2����c��CO��
��4��ij�¶��£�ƽ��Ũ�ȷ�����ʽ��c��CO2����c��H2����c��CO����c��H2O�������жϴ�ʱ���¶�Ϊ???????�档
�ο��𰸣���1 �� �����������1��ƽ�ⳣ����ָ��һ�������µĿ��淴Ӧ�У�����Ӧ�ﵽ��ѧƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը��ݷ���ʽ��֪��ƽ�ⳣ���ı���ʽΪ �����������1��ƽ�ⳣ����ָ��һ�������µĿ��淴Ӧ�У�����Ӧ�ﵽ��ѧƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը��ݷ���ʽ��֪��ƽ�ⳣ���ı���ʽΪ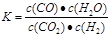
��2���������ݿ�֪�����¶ȵ�����ƽ�ⳣ�������������¶ȣ�ƽ��������Ӧ�����ƶ������Է�Ӧ�����ȷ�Ӧ��
��3����һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ������Ϊ0�����������ʵ�Ũ�Ȼ��������ٷ����仯��״̬���ǻ�ѧƽ��״̬������b��ȷ����Ӧǰ��������䣬����ѹǿʼ���Dz���ģ�a����ȷ��C�з�Ӧ���ʵķ������෴�ģ�����������֮������Ӧ�Ļ�ѧ������֮�ȣ�c��ȷ��d�з�Ӧ���ʵķ�����ͬ�����Բ���˵������ѡbc��
��4����c��CO2����c��H2����c��CO����c��H2O��ʱK��1�������¶���830�档
�����Ѷȣ���
2������� (9��)��һ����ɫ����μӵĿ��淴Ӧ�У���ϵ����ɫ�仯��������˵��ƽ��Ľ�����ƽ����ƶ�������������ɫ�仯�Ĺ۲����ܵ��۲�Ƕȼ��������̵IJ�ͬ�������仯����ͼ��ʾ����һ���¶ȡ�ѹǿ�£������IJ���ԲͲ��װ��NO2��N2O4�Ļ������100ml����ʹ���淴Ӧ2NO2 N2O4�ﵽƽ�⡣��ע�⣺����b��һԲ���棬��ɫ��dz���Կ�����ɫ�����ڽ����ϵ�ͶӰ���ܶȴ�С�� N2O4�ﵽƽ�⡣��ע�⣺����b��һԲ���棬��ɫ��dz���Կ�����ɫ�����ڽ����ϵ�ͶӰ���ܶȴ�С��
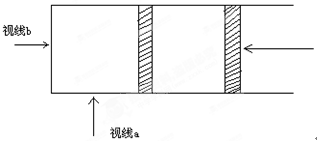
�Ž��������ͻȻѹ����50mL��ͨ������a����۲쵽��ƽ����ϵ����ɫ�仯��____________����������b����۲쵽��ƽ����ϵ����ɫ�仯��________________��˵����ɴ�a��b ��ͬ����۲����ɫ�仯���Ʋ�ͬ��ԭ����_________________________________________________________��
�ƽ�������建��ѹ����50mL����������a����۲쵽����ɫ�仯Ϊ________________________-��
��������������������ֲ�ͬ��ѹ��������������ͬ�¶Ⱥ�50mL�����״̬�´ﵽƽ�⣬���ʱƽ����ϵ��ƽ��������M1��M2�Ĺ�ϵΪ_______________-��������ɫ___________________(���ͬ����ͬ��)
������ͬ�¶ȡ�ѹǿ�£����������ֻװ��N2O4����ƽ����ظ�����ʵ�飬�����Ƿ���ͬ____________��
����NO2����N2O4�Ŀ��淴Ӧ��淴Ӧ��??????????????(�����ȡ�����)��Ӧ��2NO2 (g)?? N2O4(g) ?��ѹ��ʱ��ƽ����ϵ��???????????????�����ա��ų���������
�ο��𰸣���1���ȱ�����dz??????������dz?????��a����ѹ��
���������
��1���ȷ��������仯����ɫ����ٷ�����ѧ�仯��ƽ�������������С�ķ����ƶ�����ɫ��dz��a����۲��ȱ�����dz?????b����۲콥����dz?????��a����ѹ��������Ũ�ȸı䡢��b����ѹ��ʱ����ɫ����Ũ����һ���ģ�2�֣�
��2����������??????
��3��������ƽϡ�ǵ�Чƽ�⣺M1=M2?????��ͬ
��4��������������ƽ���������ƽ�⣬������ͬ������ƽϡ�ǵ�Чƽ�⣺��ͬ
��5������???�ų�
�����Ѷȣ�һ��
3������� ��6�֣�������Һ�н��еķ�Ӧ��FeCl3+3KSCN===Fe��SCN��3+3KCl,����������һ��ʱ��
��1������Һ�м���������KCl���壬��Һ����ɫ_______
��2������Һ�м�������KSCN���壬��Һ����ɫ_______
��3����ˮϡ��ʱ����ѧƽ����_______�ƶ�
�ο��𰸣���1������??��2������???��3���淴Ӧ
����������÷�Ӧ�����ӷ���ʽΪFe3����3SCN��=Fe(SCN)3����������Һ�м���������KCl����ʱ��ƽ�ⲻ�ƶ�����Һ��ɫ���䣻����Һ�м�������KSCN���壬ƽ��������Ӧ�����ƶ�����ɫ���ϡ�ͣ������ʵ�Ũ�Ƚ��ͣ���ɫ��dz.��ƽ�����淴Ӧ�����ƶ���
�����Ѷȣ�һ��
4������� ��6�֣�һ�������£������Ϊ3 L���ܱ������У�һ����̼��������Ӧ���ɼ״�������ΪCu2O/ZnO����CO(g)��2H2(g)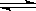 CH3OH(g) CH3OH(g)
��������������и�С�⣺
��1����500�棬�ӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v(H2)��??????????????????��
������ͼ�г��ֵ���ĸ��ʾ��

��2������������ ���������£��Դ���E�����ϵ���ѹ����ԭ����1/2�������йظ���ϵ��˵����ȷ����????????????????????�� ���������£��Դ���E�����ϵ���ѹ����ԭ����1/2�������йظ���ϵ��˵����ȷ����????????????????????��
a��������Ũ�ȼ�С?????????????? b������Ӧ���ʼӿ죬�淴Ӧ����Ҳ�ӿ�
c���״������ʵ�������?????????? d������ƽ��ʱn(H2)/n(CH3OH)����
��3�����о�����Ӧ������������õ�ΪC u2O����Ӧ��ϵ�к�����CO2������ά�ִ���Cu2O�������䣬ԭ���ǣ�??????????????????????���û�ѧ����ʽ��ʾ���� u2O����Ӧ��ϵ�к�����CO2������ά�ִ���Cu2O�������䣬ԭ���ǣ�??????????????????????���û�ѧ����ʽ��ʾ����
��4����Դ����������������ٵ��ش���⣬�״���δ������Ҫ����Դ���ʡ������£�1g�״���ȫȼ������Һ̬ˮʱ�ų�22. 7kJ��������д���״�ȼ���ȵ��Ȼ�ѧ����ʽ???????????��
�ο��𰸣�
 ����������� �����������
�����Ѷȣ�һ��
5��ѡ���� ��һ���¶��£���a L�ܱ������м���1 mol X�����2 mol Y���壬�������·�Ӧ��X��g����2Y��g��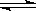 2Z��g�����˷�Ӧ�ﵽƽ��ı�־��?? 2Z��g�����˷�Ӧ�ﵽƽ��ı�־��??
A��������ѹǿ����ʱ��仯 |