��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ����β���к���CO��NO2���ж����壬��������װβ������װ�ã���ʹ�ж��������Ӧת��Ϊ�����塣����β����CO��H2O(g)��һ�������¿��Է�����Ӧ��
CO(g)��H2O(g) CO2(g)��H2(g)��H��0��820 ��ʱ�ڼס��ҡ������������ܱ������У���ʼʱ�����±�����Ͷ�ϣ��ﵽƽ��״̬��K��1.0��
CO2(g)��H2(g)��H��0��820 ��ʱ�ڼס��ҡ������������ܱ������У���ʼʱ�����±�����Ͷ�ϣ��ﵽƽ��״̬��K��1.0��
��ʼ���ʵ���
| ��
| ��
| ��
|
n(H2O)/mol
| 0.10
| 0.20
| 0.20
|
n(CO)/mol
| 0.10
| 0.10
| 0.20
?
��1���÷�Ӧ��ƽ�ⳣ������ʽΪ????????????????????????????????��
��2��ƽ��ʱ����������CO��ת������???????���Ƚ�����������CO��ת���ʣ���???????�ף���???????��(�>������������<��)��
��3���������У���Ҫͨ���ı��¶ȣ�ʹCO��ƽ��ת�����������¶���Ҫ���Ͳ��ܴﵽ�����º��ƽ�ⳣ��K?????(���������С�����䡱)��
�ο��𰸣���1��K�� ��������� ���������
�����������1����ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�������CO��g��+H2O��g�� CO2��g��+H2��g����֪���÷�Ӧ��ƽ�ⳣ������ʽΪ��K�T CO2��g��+H2��g����֪���÷�Ӧ��ƽ�ⳣ������ʽΪ��K�T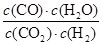 �� ��
��2�����������CO���ĵ����ʵ���Ϊx
CO��g��+H2O��g�� CO2��g��+H2��g�� CO2��g��+H2��g��
��ʼ����mol��0.1???? 0.1??????0?????? 0
�仯����mol��x??????x??????? x?????? x
ƽ������mol��0.1-x?? 0.1-x???? x?????? x
��K= ��1 ��1
���x=0.5�����Լ�������CO��ת����=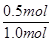 ��100%=50%�� ��100%=50%��
����Ͷ�����֪�������൱���ڼĻ�����������ˮ������Ͷ�ϣ����Ի�ʹ��һ����̼��ת��������װ��Ͷ���Ǽ�װ�õ�2�������ڻ�ѧ��Ӧǰ��ϵ���Ͳ���ķ�Ӧ��˵��������ƽ���ǵ�Ч�ģ�������������£�ת��������ȵġ�
�۱������У�ͨ���ı��¶ȣ�ʹCO��ƽ��ת����������Ҫʹ��ѧƽ�����������ƶ������ڸ÷�ӦΪ���ȷ�Ӧ��Ҫ����һ����̼��ת���ʣ�Ӧ�ý����¶ȣ�����ƽ�����������ƶ�����Ӧ��Ũ�ȼ�С��������Ũ��������÷�Ӧ�Ļ�ѧƽ�ⳣ������
�����Ѷȣ���
2������� . (14��)��֪A(g)+B(g) C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£� C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
|�¶�/ ��
| 700
| 900
| 830
| 1000
| 1200
| ƽ�ⳣ��
| 1.7
| 1.1
| 1.0
| 0.6
| 0.4
�ش��������⣺
(1)�÷�Ӧ��ƽ�ⳣ������ʽK=?????????????����H????0���<���� >���� =��)��
(2)830��ʱ����һ��5 L���ܱ������г���0.20mol��A��0.80mol��B���練Ӧ��ʼ6s��A��ƽ����Ӧ����v(A)=0��003 mol��L-1��s-1������6sʱc(A)=??????mol��L-1�� C�����ʵ���Ϊ??????mol������Ӧ��һ��ʱ��ﵽƽ��ʱA��ת����Ϊ?????�������ʱ����ܱ��������ٳ���1 mol�����ƽ��ʱA��ת����Ϊ?????????��
(3)�жϸ÷�Ӧ�Ƿ�ﵽƽ�������Ϊ??????(����ȷѡ��ǰ����ĸ)��???
a��ѹǿ����ʱ��ı�??? b.������ܶȲ���ʱ��ı�
c. c(A)����ʱ�ʸı�???? d.��λʱ��������c��D�����ʵ������???
(4)1200��ʱ��ӦC(g)+D(g) ?A(g)+B(g)��ƽ�ⳣ����ֵΪ?????????????�� ?A(g)+B(g)��ƽ�ⳣ����ֵΪ?????????????��
�ο��𰸣�����14�֣�
(1) �����������1��ƽ�ⳣ������һ�������£����淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը÷�Ӧ��ƽ�ⳣ������ʽK= �����������1��ƽ�ⳣ������һ�������£����淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը÷�Ӧ��ƽ�ⳣ������ʽK=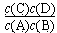 �����ݱ������ݿ�֪�������¶ȣ�ƽ�ⳣ����С����˵�������¶�ƽ�����淴Ӧ������У��������Ӧ�Ƿ��ȷ�Ӧ������H<0�� �����ݱ������ݿ�֪�������¶ȣ�ƽ�ⳣ����С����˵�������¶�ƽ�����淴Ӧ������У��������Ӧ�Ƿ��ȷ�Ӧ������H<0��
��2��6s��A��ƽ����Ӧ����v(A)=0��003 mol��L-1��s-1����������A��Ũ����0.018mol/L��A����ʼŨ����0.20mol��5L��0.04mol/L�����Դ�ʱA��Ũ����0.04mol/L��0.018mol/L��0.022mol/L�����ݷ���ʽ��֪��C�����ʵ���Ũ����0.018mol/L������C�����ʵ�����0.018mol/L��5L��0.09mol����A��ת������x����ƽ��ʱABCD�����ʵ����ֱ��ǣ�0.2��0.2x��mol����0.8��0.2x��mol��0.2xmol��0.2xmol������ƽ�ⳣ������ʽ��֪0.2x��0.2x����0.2��0.2x������0.8��0.2x�������x��0.8����ת������80���������ʱ����ܱ��������ٳ���1 mol�������ƽ�ⲻ�ƶ���ת���ʲ��䡣
��3����һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ������Ϊ0������Ӧ��ϵ�и������ʵ�Ũ�Ȼ������ٷ����仯��״̬����Ϊ��ѧƽ��״̬������ѡ��c��ȷ����Ӧǰ��������䣬���ѹǿʼ���Dz���ģ�a����ȷ���ܶ��ǻ�����������������ݻ��ı�ֵ���ڷ�Ӧ�������������ݻ�ʼ���Dz���ģ�b����ȷ��d�з�Ӧ���ʵķ�������ͬ�ģ�����֮������Ӧ�Ļ�ѧ������֮�ȣ����d�еĹ�ϵʼ���dz���������ȷ����ѡc��
��4���淴Ӧ��ƽ�ⳣ��������Ӧƽ�ⳣ���ĵ�������˸÷�Ӧ��ƽ�ⳣ����1��0.4��2.5��
�����Ѷȣ�һ��
3��ѡ���� ��ҵ�������е�һ����Ҫ��Ӧ��SO2��400��500���µĴ�������2SO2��O2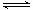 2SO3������һ�����ȵĿ��淴Ӧ�������Ӧ���ܱ������н��У������й�˵���У�������� 2SO3������һ�����ȵĿ��淴Ӧ�������Ӧ���ܱ������н��У������й�˵���У��������
A��ʹ�ô�����Ϊ�˼ӿ췴Ӧ���ʣ��������Ч��
B�������������£�SO2������100%��ת��ΪSO3
C���ﵽƽ��ʱ���ı䷴Ӧ����������һ���̶��ϸı�÷�Ӧ�Ļ�ѧƽ��״̬
D���ﵽƽ��ʱ��SO2��Ũ����SO3��Ũ��һ�����
�ο��𰸣�D
���������
���������ʹ�ô�����Ϊ�˼ӿ췴Ӧ���ʣ��������Ч�ʣ�A��ȷ���÷�Ӧ�ǿ��淴Ӧ�����������������£�SO2������100%��ת��ΪSO3��B��ȷ��ƽ��״̬��һ�������µģ�����ı����������ƽ��״̬���Է����仯��C��ȷ����һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ������Ϊ0������Ӧ��ϵ�и������ʵ�Ũ�Ȼ������ٷ����仯��״̬����Ϊ��ѧƽ��״̬��ƽ��ʱŨ�Ȳ��ٷ����仯��������֮���Ũ�Ȳ�һ����Ȼ�����ij�ֹ�ϵ�����ѡ��D����ȷ����ѡD��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣���ؿ���ѧ���Կ��淴Ӧƽ��״̬�ص��Լ����������ƽ��״̬Ӱ�����Ϥ�˽�̶ȣ������ڵ���ѧ����ѧϰ��Ȥ�����ѧ����ѧϰЧ�ʺ�Ӧ��������
�����Ѷȣ�һ��
4������� ��24�֣�ÿ��3�֣�
(1)��4molSO2��2molO2����2L���ܱ������У���һ�������·�����Ӧ����10s��ﵽƽ�⣬���SO3 ��Ũ��Ϊ0.6mol��L��1����ش��������⣺ ��Ũ��Ϊ0.6mol��L��1����ش��������⣺
����O2��ʾ�ķ�Ӧ��ƽ������Ϊ___________________________ __________ __________
��ƽ��ʱSO2��ת����______________________________________
��ƽ��ʱSO3���������Ϊ___________________________
��10sʱO2��Ũ��Ϊ_____________________________________________
(2)��֪ij���淴ӦmA(g)��nB(g)  ?qC(g)���ܱ������н��С� ?qC(g)���ܱ������н��С�
��ͼ��ʾ��Ӧ�ڲ�ͬʱ��t���¶�T��ѹǿP�뷴Ӧ��B�����
�����Ĺ�ϵ���ߡ�����ͼ�����
�ٻ�ѧ�������Ĺ�ϵ:m��n______q��(� ����.������������ ����.������������
�ڸ÷�Ӧ������ӦΪ___________��Ӧ��������ȡ����ȡ���
(3)��FeCl3+3KSCN Fe(SCN)3+3KCl��ƽ����ϵ�У��ش��������⣺ Fe(SCN)3+3KCl��ƽ����ϵ�У��ش��������⣺
���������������������
������Һ�м���������KSCN���壬ƽ��???? ______________�ƶ���
������Һ�м���������KCl���壬 ƽ��????? _____________�ƶ��� ƽ��????? _____________�ƶ���
�ο��𰸣���1�� ��0.0 ����������� �����������
�����Ѷȣ�һ��
5������� ��12�֣������Ϊ2L�Ĺ̶��ܱ�������ͨ��3molX���壬��һ���¶��·������·�Ӧ��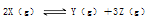
��1����5min���ƽ�⣬��ʱ������ѹǿΪ��ʼʱ��1.2��������Y��ʾ������Ϊ____________mol(L��min)��
��2����������Ӧ�ڼס��ҡ��������ĸ�ͬ�����ܱ������н��У���ͬһʱ���ڲ�õķ�Ӧ���ʷֱ�Ϊ���ף��ͣ�X����3.5mol(L��min)���ң��ͣ�Y����2mol(L��min)�������ͣ�Z����4.5mol(L��min)�������ͣ�X����0.075mol(L��s)��������������ͬ���¶Ȳ�ͬ���¶��ɸߵ��͵�˳���ǣ�����ţ�________________��
��3������ﵽ��1����ƽ����ϵ�г��뵪������ƽ�� ��___������ҡ���������ͬ���ƶ��������ﵽ��1����ƽ����ϵ�����߲��ֻ�����壬��ƽ����___�ƶ��� ��___������ҡ���������ͬ���ƶ��������ﵽ��1����ƽ����ϵ�����߲��ֻ�����壬��ƽ����___�ƶ���
��4��������ͬ��������ﵽ��1������ƽ����ϵ���ٳ���0.5molX���壬��ƽ���X��ת�����루1����ƽ����X��ת�������___
A����ȷ��
B��ǰ��һ�����ں���
C��ǰ��һ�����ں���
D��ǰ��һ��С�ں���
��5���������¶Ⱥ�ѹǿ���䣬��ʼʱ����X��Y��Z���ʵ����ֱ�Ϊamol��bmol��cmol����ƽ��ʱ���루1����ƽ���Ч����a��b��cӦ����Ĺ�ϵΪ____________��
��6���������¶Ⱥ�������䣬��ʼʱ����X��Y��Z���ʵ����ֱ�Ϊamol��bmol��cmol����ƽ��ʱ���루1����ƽ���Ч������ʼʱά�ֻ�ѧ��Ӧ���淴Ӧ������У���c��ȡֵ��ΧӦΪ______________��
�ο��𰸣�(14��)��1��0.03???��2����>��>��&
�����������
�����Ѷȣ���
|
|