��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��6�֣���ú��Ϊȼ�Ͽ�ͨ����������;����
;���� C(s)+ O2(g)=====CO2(g)����H1��0 ��
;���� ���Ƴ�ˮú����
C(s)+H2O(g)=====CO(g)+H2(g)����H2��0 ��
��ȼ��ˮú����
2CO(g)+O2(g)=====2CO2(g)����H3��0 ��
2H2(g)+O2(g)=====2H2O(g)����H4��0 ��
��ش��������⣺
��1��;����ų�������_________(����ڡ������ڡ���С�ڡ�);����ų���������
��2����H1����H2����H3����H4����ѧ��ϵʽ��_______________��
�ο��𰸣���6�֣���1������ ��2����H1=��H2+
���������
�����������1���ɸ�˹���ɿ�֪��;�����;����Ӧ���״̬���������״̬��ͬ���ʱ���ͬ����Ӧ����ͬ����2���ɸ�˹���ɵæ�H1=��H2+ (��H3+��H4)��
(��H3+��H4)��
���㣺�ʱ䡢��˹����
�����Ѷȣ�һ��
2��ѡ���� ����������ȷ����
A.������ֻ�������ԣ�������ֻ�л�ԭ��
B.������������������������
C.��8NH3+3Cl2�TN2+6NH4Cl��Ӧ�У��������뻹ԭ�����ʵ���֮����2��3
D.��֪��ԭ�ԣ�Fe2+��Br-����֪��Ӧ2Fe3++2Br-�T2Fe2++Br2������
�ο��𰸣�D
���������������A����Ԫ����ۿ��Ծ��������ԣ�������ͼ۾��л�ԭ�Է�����
B������������ԭ��Ӧ��������������Ԫ�ػ��ϼ۵ı仯�йأ�ֻҪ����Ԫ�ػ��ϼ۽��ͣ��Ϳ�������������
C����ע���ϼۣ������������ͻ�ԭ�������ʵ�����
D����������ԭ��Ӧ����ѭǿ�����ɣ���ԭ���Ļ�ԭ�Դ��ڻ�ԭ��������жϣ�
���A���������м��̬������������Ҳ���л�ԭ�ԣ������ӿ����л�ԭ�ԣ�Ҳ�����������ԣ���A����
B���������������������������Ҳ�������������������������Ӧ����B����
C����8NH3+3Cl2�TN2+6NH4Cl��Ӧ�У�������Ϊ��������ԭ��Ϊ��������ע���ϼ��жϣ�����������3mol���ϼ۱仯��Ӧ����ԭ��NH32mol���ϼ۱仯��Ӧ�������������뻹ԭ�����ʵ���֮����3��2����C����
D����֪��ԭ�ԣ�Fe2+��Br-�����ݻ�ԭ���Ļ�ԭ�Դ��ڻ�ԭ�����֪��Ӧ2Fe3++2Br-�T2Fe2++Br2�������ϻ�ԭ��ǿ�������Բ����У���D��ȷ��
��ѡD��
���������⿼���˸��ݻ��ϼ۱仯�ж�������ԭ��Ӧ�ĸ��ָ���Ĺ�ϵ��������ԭ��Ӧ�Ķ������㷽������Ӧ�ܷ���е��ж����ݣ�
�����Ѷȣ���
3��ѡ���� 100g̼ȼ�����������У�COռ1/3�����CO2ռ2/3�������C(s)+ 1/2O2(g) CO(g)? ��H=��110.35kJ��mol-1,CO(g)+ 1/2O2(g)
CO(g)? ��H=��110.35kJ��mol-1,CO(g)+ 1/2O2(g) CO2(g)? ��H=��282.57kJ��mol-1������Щ̼��ȫȼ����Ƚϣ���ʧ�������ǣ�???��
CO2(g)? ��H=��282.57kJ��mol-1������Щ̼��ȫȼ����Ƚϣ���ʧ�������ǣ�???��
A��392.92kJ
B��2489.44kJ
C��784.92kJ
D��3274.3kJ
�ο��𰸣�C
���������100g̼ȼ������������CO�����ʵ���Ϊ ����Щ���ʵ���CO��ȫȼ�շų�������Ϊ
����Щ���ʵ���CO��ȫȼ�շų�������Ϊ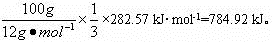
�����Ѷȣ�һ��
4��ѡ���� ��NaOH20.0g��ϡ��Һ��������ϡ���ᷴӦ���ų�28.7kJ����������ʾ�÷�Ӧ���Ȼ�ѧ����ʽ��
A��NaOH��aq����HCl��aq����NaCl��aq����H2O��l������H����28.7kJ/mol
B��NaOH��aq����HCl��aq����NaCl��aq����H2O��l������H����28.7kJ/mol
C��NaOH��aq����HCl��aq����NaCl��aq����H2O��l������H����57.4kJ/mol
D��NaOH��aq����HCl��aq����NaCl��aq����H2O��l������H����57.4kJ/mol
�ο��𰸣�D
���������
��ȷ�𰸣�D
NaOH20.0g��0.5mol���ų�28.7kJ��������1molNaOH��Ӧ�����57.4kJ�����ȷ�Ӧ�ġ�HΪ��ֵ������������D��ȷ��
�����Ѷȣ�һ��
5��ѡ���� ��ӦA2+B2 2AB���¶Ⱥ�ѹǿ�ı������£�����AB�����������ͼ��ʾ��aΪ500�棬bΪ
2AB���¶Ⱥ�ѹǿ�ı������£�����AB�����������ͼ��ʾ��aΪ500�棬bΪ
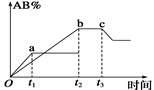
300��ʱ�����cΪ300��ʱ��ʱ��t3��ʼ�������м�ѹ���������������
����ȷ���ǣ� ��
A��A2��B2��AB��Ϊ���壬����Ӧ����
�ο��𰸣�
���������
�����Ѷȣ�һ��