微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 对0.1mol?L-1的醋酸溶液进行以下操作,下列分析判断正确的是( )
A.加入少量0.1mol?L-1的硫酸,水电离产生的c(H+)减小
B.升高温度,溶液的pH会增大
C.加入少量固体NaOH,溶液中c(CH3COO-)+c(OH-)>c(Na+)+c(H+)
D.与0.1mol?L-1的NaOH溶液等体积混合后,溶液中c(CH3COO-)=c(Na+)
参考答案:A
本题解析:
本题难度:简单
2、选择题 pH=l的两种一元酸HX与HY溶液,分别取50mL加入足量的镁粉,充分反应后,收集到H2体积分别为V(HX)和V(HY).若V(HX)>V(HY),则下列说法正确的是( )
A.HX可能是强酸
B.HX的酸性比HY的酸性弱
C.两酸的浓度大小为c(HX)<c(HY)
D.将两种一元酸均稀释100倍,稀释后两溶液的pH均为3
参考答案:B
本题解析:
本题难度:简单
3、选择题 相同物质的量浓度的下列化合物的水溶液,按PH减小顺序排列是( )
A.NaHSO4 CH3COONa? NH4Cl NaNO3
B.NaNO3 CH3COONa? NaHSO4???? NH4Cl
C.CH3COONa NaNO3? NH4Cl NaHSO4
D.NaNO3 CH3COONa? NH4Cl????NaHSO4
参考答案:C
本题解析:
本题难度:一般
4、填空题 2013年1月27日百度新闻资讯中报道,活性氧化锌是一种多功能性的新型无机材料,其颗粒大小约在1~100纳米。云南化工冶金研究所采用湿化学法(NPP-法)制备纳米级活性氧化锌,可用各种含锌物料为原料,采用酸浸出锌,经过多次净化除去原料中的杂质,然后沉淀获得碱式碳酸锌,最后焙解获得活性氧化锌,化学工艺流程如下:
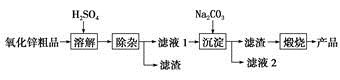
(1)通过________可以检验流程中滤液2中含有Na+。
(2)上述流程图中pH=12的Na2CO3溶液中c(CO32- )=0.50 mol/L,c(HCO3- )=1×10-2 mol/L,则c(Na+)∶c(OH-)=________。
(3)“溶解”后得到的酸性溶液中含有Zn2+、SO42- ,另含有Fe2+、Cu2+等杂质。先加入________(填“Na2CO3”或“H2SO4”)调节溶液的pH至5.4,然后加入适量KMnO4,Fe2+转化为Fe(OH)3,同时KMnO4转化为MnO2。经检测溶液中Fe2+的浓度为0.009 mol・L-1,则每升溶液中至少应加入________mol KMnO4。
(4)已知常温下,Cu(OH)2的溶度积常数Ksp=2×10-20。溶液中杂质Cu2+浓度为0.002 mol・L-1,若要生成沉淀,则应调节溶液的pH大于________。
(5)“沉淀”得到ZnCO3・2Zn(OH)2・H2O,“煅烧”在450~500 ℃下进行,“煅烧”反应的化学方程式为:_____________________________________。
参考答案:(1)焰色反应
(2)102 ∶1
(3)Na2
本题解析:(1)检验溶液中含有Na+,常用焰色反应。
(2)根据物料守恒,c(Na+)= 2×0.51 mol/L=1.02 mol/L,pH=12,c(OH-)=0.01 mol/L。
(3) 溶解后得到酸性溶液,要调节溶液的pH至5.4,需要升高pH,故应加入Na2CO3 n(Fe2+)= 0.009 mol, 根据电子得失守恒,则n(KMnO4)=0.003 mol。
(4) )根据信息:当c(Cu2+)・[c(OH-)]2=2×10-20时开始出现沉淀,则c(OH-)=10-8 mol・L
本题难度:一般
5、填空题 在a、b两支试管中,分别装上形态相同、质量相等的一颗锌粒,然后向两支试管中分别加入相同物质的量、相同体积的稀盐酸和稀醋酸。填写下列空白:?
(1)a、b两支试管中的现象:相同点是_______________;不同点是_______________。原因是______________________________。
(2)a、b两支试管中生成气体的体积开始时是a______b,反应完毕后生成气体的总体积是a_______b,原因是______________________________。(填“大于”、“小于”、“等于”)?
参考答案:(1)都产生气泡,Zn溶解;a产生气泡、Zn溶解速度都快;H
本题解析:
本题难度:一般