微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (3分)请自行设计实验,用至少两种方法证明盐酸的酸性比醋酸的酸性强?
可供选者选择的试剂:0.1mol/L的HCl 0.1mol/L的CH3COOH 0.1mol/L 的NaOH 0.1mol/L的CH3COONa CaCO3粉末 PH试纸 蒸馏水 酚酞试液 石蕊试液 玻璃仪器自行选择。
参考答案:
方法一:分别取两张PH试纸放在玻璃片上,用玻璃棒分别
本题解析:
试题分析:本题考察学生对于化学实验知识的掌握程度,以及学生自行设计实验方案的能力,属于开放性试题,对于学生的综合测评较为全面。
考点:化学实验以及仪器组装。
点评:本题属于实验开放题,在比较酸性强弱中有很多方法,可以测定同浓度溶液的pH,也可以利用强酸制弱酸来设计,答案不限。
本题难度:一般
2、选择题 在NH3.H2O?NH
?
+4
+OH-形成的平衡中,要使NH3?H2O的电离程度及c(OH-)都增大,可采取的措施是( )?
A.通入HCl?
B.加少量NaOH固体?
C.加少量氯化铵固体?
D.加热
参考答案:A.通入氯化氢气体,氯化氢和氢氧根离子反应,促进氨水电离,但
本题解析:
本题难度:简单
3、选择题 下列说法中,错误的是[???? ]
A. NaHCO3溶液中碳元素主要以HCO3-存在
B. Na2CO3溶液中滴加酚酞呈红色,加热红色变深
C. NH4Cl溶液呈酸性这一事实能说明一水合氨为弱碱
D. 在稀醋酸中加醋酸钠固体能促进醋酸的电离
参考答案:D
本题解析:
本题难度:一般
4、填空题 有浓度为0.1 mol?L-1的盐酸、硫酸、醋酸三种溶液,试回答:
(1)三种溶液中c(H+) 依次为a mol?L-1,b mol?L-1,c mol?L-1,其大小顺序为__________。
(2)等体积的以上三种酸分别与过量的NaOH 溶液反应,生成的盐的物质的量依次为n 1mol,n2 mol,n3 mol,它们的大小关系为____________。
(3)中和一定量NaOH溶液生成正盐时,需上述三种酸的体积依次是V1L、V2L、V3L,其大小关系为____________。
(4)与锌反应时产生氢(气)的速率分别为v1、v2、v3,其大小关系为____________
参考答案:(1)a= 本题解析:盐酸是一元强酸,硫酸是二元强酸,醋酸是一元弱酸,存在电离平衡。所以
本题解析:盐酸是一元强酸,硫酸是二元强酸,醋酸是一元弱酸,存在电离平衡。所以
(1)a=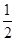 b>c
b>c
(2)由于酸根的物质的量都是相同的,因此生成的盐的物质的量也是相同的,即n1=n2=n3。
(3)在氢氧化钠相同的条件下,需要硫酸的量少,因此答案是V1=V3=1/2V2。
(4)氢离子浓度越大,反应速
本题难度:一般
5、填空题 (9分)25℃时,有0.01 mol?L-1的醋酸溶液,试回答下列问题:
(1)写出醋酸的电离平衡常数表达式
(2)达平衡时,溶液中氢离子浓度是多少?(25℃时,醋酸的电离平衡常数为1. 75×10 -5)
(3)当向该溶液中加入一定量的盐酸时,溶液中的c(H+)、c (CH3COO-)、c (CH3COOH) 是否又发生变化? 电离常数是否发生变化? 为什么 ?
参考答案:(1)K=  本题解析:(1)电离平衡常数和化学平衡常数是类似的,所以醋酸的电离平衡常数表达式为K=
本题解析:(1)电离平衡常数和化学平衡常数是类似的,所以醋酸的电离平衡常数表达式为K= 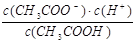 。
。
(2)醋酸的电离方程式为CH3COOH 本题难度:一般
本题难度:一般