微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (9分)某研究性学习小组利用废铜制取CuSO4:
(1) 甲学生进行了下列实验:取含6.4g铜的废铜和10ml 18ml・L-1浓硫酸放在圆底烧瓶中共热,起到反应完毕,最后发现烧瓶中还有铜片剩余。他根据自己所学的化学知识,认为烧瓶中还有较多的硫酸剩余。你认为他的判断是否正确?????????,其理由是:????????????????????
???????????????????????????????????????????????。
 写出相关的化学方程式:???????????????????????????????????????????????。
写出相关的化学方程式:???????????????????????????????????????????????。
(2) 乙同学认为甲设计的实验方案不好,他自己设计的思路是:2Cu+O2==2CuO;CuO+H2SO4
==CuSO4+H2O。对比甲的方案,乙同学的优点是:?????????????????????????????????????
??????????????????????????????????????????????。
(3) 丙同学采用向含有废铜屑的热的稀H2SO4中,不断通入空气也能制备CuSO4,请写出相关的化学方程式:????????????????????????????????????????????????????????????????????。
参考答案:(1)是(1分),随着反应的进行硫酸浓度变小,稀硫酸不与铜反
本题解析:(1)由于只有浓硫酸才能和铜反应。而随着反应的进行硫酸浓度变小,稀硫酸不与铜反应,反应的方程式为Cu+2H2SO4(浓)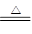 CuSO4+SO2+2H2O。
CuSO4+SO2+2H2O。
(2)浓硫酸直接核铜反应,会产生SO2,污染环境,且硫酸的用量也多。
(3)因为在加热的条件下,氧气能把铜氧化,生成氧化铜,氧化铜核硫酸反应即生成硫酸铜。方程式为2Cu+O2+2H2SO4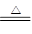 2CuSO4 +2H2O。
2CuSO4 +2H2O。
本题难度:简单
2、实验题 (15分)某化学小组为测定加碘盐中KIO3的质是分数并制备少量KIO3,进行了如下实验。
I .测定加碘盐中KIO3的质量分数(杂质不发生反应)
已知: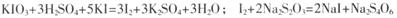
步骤一:准确称取a g加碘盐,配制成250 mL溶液;
步骤二:取所配溶液25.00 mL于锥形瓶中,加稀硫酸酸化,再加入足量KI溶液;
步骤三:以淀粉为指示剂,用c mol.L-1的Na2S2O3溶液滴定步骤二所得溶液至终点,记录数据。重复滴定2次,平均消耗Na2S2Or溶液12.00 mL。
(1) 步骤一中配制250mL溶液用到的玻璃仪器除烧杯、玻璃棒和量筒外,还有____________
(2) 步骤三中到达滴定终点时的现象为____________
(3) 实验测得此加碘盐中KIO3的质量分数="______" ______ (KIO3的相对分子质量为214)。
II.实验室制备KIO3
已知:碘酸盐可以用氯气在碱性溶液中氧化碘化物得到。
该化学小组通过以下装置制备KIO3
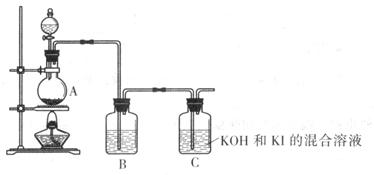
(4) 装置A中反应的离子方程式为____________
(5) 装置B中的试剂为____________
(6) 写出装置C中生成KIO3的离子方程式____________。
(7) 上述实验装置存在一处明显缺陷,请指出: __________________。
参考答案:(1)250mL容量瓶、胶头滴管(2分,各1分,不写250m
本题解析:(1)考查一定物质的量浓度溶液的配制,根据实验原理和已知的仪器可知,还缺少的是250mL容量瓶、胶头滴管。
(2)由于淀粉和碘反应显蓝色,所以终点时的实验现象是溶液蓝色褪色,半分钟内不恢复蓝色。
(3)利用关系式进行计算。根据方程式可知KIO3~3I2~6Na2S2O3,所以25ml溶液中碘酸钾的物质的量是0.012cmol÷6=0.002cmol,所以此加碘盐中KIO3的质量分数=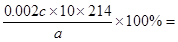
(4.28c)/a×100%。
(4)装置A是制取氯气的发生装置,方程式为MnO2+4H++2Cl-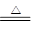 Mn2++Cl2↑+2H2O。
Mn2++Cl2↑+2H2O。
(5)由于盐酸易挥发,所以制取的氯气中含有氯化氢,而氯化氢能和氢氧化钠反应,导致实验失败,所以再通入装置C之前,需要除去氯化氢,可利用饱和食盐水除去氯化氢。
(6)氯气的还原产物是氯离子,所以根据反应物和生成物可知,方程式为I-+3Cl2+6OH-=IO3-+6 Cl-+3H2O。
(7)由于氯气有毒,所以必需有尾气处理装置,否则易造成环境污染。
本题难度:一般
3、实验题 (2014届山东省泰安市高三第一轮复习质量检测化学试卷)
碘化钠是制备无机和有机碘化物的原料,在医药上用作祛痰剂和利尿剂等。工业上用铁屑还原法制备NaI,其主要流程如下图:
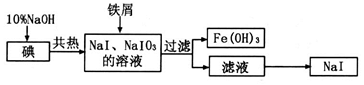
(1)写出铁屑转化为Fe(OH)3反应的离子方程式:????????????????????????????????。
(2)判断碘已完全反应的方法是????????????????????????????????????。
(3)由滤液得到NaI晶体的操作是????????????????????????????????????。
(4)测定产品中NaI含量的方法是:
a.称取3.000g样品溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用0.100mol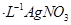 溶液滴定至终点,消耗
溶液滴定至终点,消耗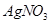 溶液体积的平均值为19.00mL。
溶液体积的平均值为19.00mL。
①上述测定过程所需仪器中,需要检查是否漏液的仪器有?????????????????????????,
其中使用前需进行润洗的仪器是????????????????????????;
②上述样品中NaI的质量分数为??????????????????????????????????????????????。
参考答案:(1)2Fe+IO3?+3H2O=2Fe(OH)3↓+I?(
本题解析:
(1)根据流程图可以看出,NaOH与I2共热反应可生成NaI和NaIO3,加入铁屑生成了Fe(OH)3和NaI,所以铁屑转化为Fe(OH)3反应的离子方程式为:2Fe+IO3?+3H2O=2Fe(OH)3↓+I?
(2)利用I2能使淀粉变蓝的现象判断碘是否反应完全:用小试管取溶液少许,向其中滴加几滴淀粉溶液,如果溶液不变蓝色,则证明碘反应完全。
(3)NaI溶液在蒸发水时,没有副反应发生,所以采用蒸发、结晶的方法得到NaI晶体。
(4)①250mL容量瓶、滴定管需要检查是否漏液,滴定管在使用前需要进行润洗。
②根据AgNO3的物质的量求算NaI的物质的量,所以样品中NaI的质量分数为:0.100mol/L×0.019L×150g/mol×10÷3.000g×100%=95%
本题难度:一般
4、填空题 某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
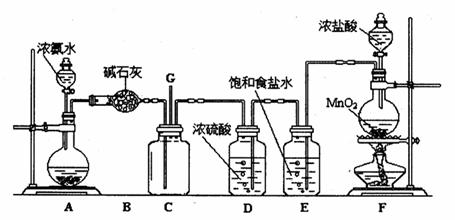
请回答下列问题:?
(1) F中发生反应的化学方程式为??????????????????????????????????????????????????;
(2)C中发生的反应为:8NH3 + 3Cl2===? N2 + 6NH4Cl ,其中氧化剂与还原剂的物质的量之比为?????????;当a mol氯气参加反应时,转移的电子总数为b个,则阿伏加德罗数常数为?????????mol-1(用含a、b的代数式表示);
(3) 将F制得的氯气通人含74g Ca(OH)2的石灰乳中,最多可制得漂白粉??????????????g。
参考答案:
(1)? MnO2 + 4HCl(浓) ![]()
本题解析:
试题分析:(1)F中是浓盐酸与二氧化锰反应制得氯气的反应。(2)氨气中氮元素从-3价升高到0价,作还原剂。但是8个氮原子中只有两个变价。而氯气全部都变成了氯化铵,所以氧化剂与还原剂之比为3:2。(3)a mol氯气反应,则转移的电子为2a mol ,而电子总数为b个,则阿伏伽德罗常数为b/2a。(3)74g的 Ca(OH)2物质的量为:1mol,则漂白粉主要成分为次氯酸,则次氯酸为1mol,共127g。
点评:本题涉及到了两个重要气体的制备实验,本题在实验装置上没有设置问题,而在方程的关于物质的量计算上有问题设置。其中利用到了元素守恒,电子得失守恒来计算。
本题难度:一般
5、选择题 为了得到比较纯净的物质,使用的方法恰当的是( ???)
A.向Na2CO3饱和溶液中,通入过量的CO2后,在减压、加热条件下,蒸发得到NaOH晶体
B.加热蒸发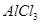 饱和溶液得纯净的
饱和溶液得纯净的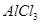 晶体
晶体
C.向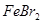 溶液中加入过量的氯水,加热蒸发得
溶液中加入过量的氯水,加热蒸发得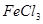 晶体
晶体
D.向Fe2(SO4)3溶液加入足量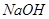 溶液,经过过滤、洗涤沉淀,再充分灼烧沉淀得
溶液,经过过滤、洗涤沉淀,再充分灼烧沉淀得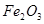
参考答案:D
本题解析:
试题分析:碳酸钠和CO2反应生成的是碳酸氢钠,得不到氢氧化钠,A不正确;B中氯化铝溶液中存在水解平衡,加热促进水解,且生成的氯化氢极易挥发,最终生成的是氢氧化铝,得不到氯化铝;同样分析,C中达到的是氢氧化铁,所以正确的答案选D。
点评:该题是中等难度的试题,试题基础性强,难度不大。主要是有利于培养学生灵活运用水解原理解决实际问题的能力。该题的关键是明确水解原理,并能结合题意灵活运用即可。
本题难度:简单