微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
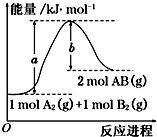
1、选择题 已知化学反应A2(g)+B2(g)═2AB(g)的能量变化如图所示,判断下列叙述中正确的是( )
A.该反应热△H=+(a-b)?kJ?mol-1
B.每生成2mol AB(g)吸收b?kJ
C.该反应中反应物的总能量高于生成物的总能量
D.断裂1mol?A-A和1mol?B-B键,放出a?kJ能量
参考答案:A、反应热△H=反应物能量总和-生成物能量总和,所以反应热△
本题解析:
本题难度:简单
2、选择题 在一个容积为2 L的恒容密闭容器中加入0.2 mol CO和0.4 mol H2,发生反应:
CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
实验测得在300℃和500℃时,甲醇的物质的量(mol)随时间的变化如下表所示。
?
| 10 min
| 20 min
| 30 min
| 40 min
| 50 min
| 60 min
|
300℃
| 0.080
| 0.120
| 0.150
| 0.168
| 0.180
| 0.180
|
500℃
| 0.120
| 0.150
| 0.156
| 0.160
| 0.160
| 0.160
???下列说法正确的是
A.该反应的ΔH>0,升高温度,化学平衡常数K增大
B.300℃时,前20 min内的反应速率v(H2)="0.003" mol·L-1·min-1
C.采取加压、增大c(H2)、加入合适的催化剂等措施都能提高CO的转化率
D.500℃时,在起始时向容器中加入0.1 mol CO和0.3 mol H2,可计算出反应达平衡后甲醇的浓度
参考答案:D
本题解析:
试题分析:A、300℃平衡时甲醇的物质的量大于500℃平衡时甲醇的物质的量,所以升高温度平衡逆向移动,正向是放热反应,ΔH<0,错误;B、300℃时,前20 min内甲醇的物质的量增加0.120mol,则氢气的物质的量减少0.240mol,浓度改变0.120mol/L,所以前20 min内的反应速率v(H2)=0.006mol·L-1·min-1,错误;C、增大c(H2),只能增大CO的转化率,而氢气的转化率降低,错误;D、由所给数据可计算500℃时的化学平衡常数,所以已知CO和H2的物质的
本题难度:一般
3、选择题 关于某一化学反应的熵变,下列说法正确的是(???)
A.△S为反应产物总熵与反应物总熵之差
B.△S与S一样随温度变化不大
C.凡是熵增加的反应一定能自发进行
D.在温度、压强一定的条件下,焓变和熵变共同决定化学反应进行的方向
参考答案:AD
本题解析:
试题分析:熵是与物质混乱度有关系的物理量,选项A正确。熵值以及熵变都是和温度有关系的,B不正确;熵增加的反应不一定能自发进行,选项C不正确;反应的自发性由焓变和熵变共同决定,即满足△G=△H-T·△S,选项D正确,因此正确的答案选AD。
点评:该题是基础性试题的考查,侧重对教材基础知识的巩固和训练,意在提高学生灵活运用基础知识解决实际问题的能力,难度不大,记住即可!
本题难度:简单
4、选择题 人们在生产和生活中认识到,几乎在所有的化学变化过程中都伴随着能量变化,例如放热、吸热、发光、放电等等。如果从能量变化的角度来认识,下面说法中正确的是[???? ]
A.化学变化都是放热的
B.反应物所含能量等于生成物所含能量
C.化学变化都是吸热的
D.化学反应前后反应物和生成物所含能量会发生变化
参考答案:D
本题解析:
本题难度:简单
5、选择题 右图是373K时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是

A.该反应的热化学方程式为:N2+3H2 2NH3△H=-92kJ·mol-1 2NH3△H=-92kJ·mol-1
B.a曲线是加入催化剂时的能量变化曲线
C.加入催化剂,该化学反应的反应热不变
D.在相同温度的条件下,在体积相同I、II两个容器中分别通入1mol N2和3 mol H2,容器I体积恒定,容器II体积可变保持恒压,则反应过程中两容器内的反应速率V(I)<V(II)
参考答案:C D
本题解析:略
本题难度:简单
|