微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (12分)能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。阅读下列有关能源的材料,回答有关问题:
(1)从能量的角度看,断开化学键要?????? _??,形成化学键要?????????。已知拆开1 mol H-H键、1 mol I-I、1 mol H-I键分别需要吸收的能量为436 kJ、151 kJ、299 kJ。则由氢气和碘反应生成1 mol HI需要?? __??(填“放出”或“吸收”)?? ___?kJ的热量。
(2)沼气是一种廉价能源,农村存在大量的秸秆、杂草等废弃物,它们经微生物发酵之后,便可产生沼气,可用来点火做饭。已知8g甲烷完全燃烧生成液态水时放出445.0kJ的热量,请写出甲烷燃烧热的热化学方程式____________________________________。
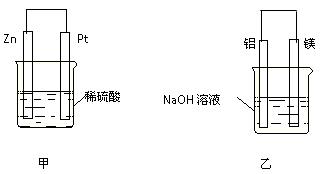
(3)在生产和生活中经常遇到化学能与电能的相互转化。
在如图甲、乙两装置中,甲中负极电极反应式为_____________________,
溶液中的阳离子向_____极移动(填“正”或“负”);乙中铝电极作__________极,发生______反应(填“氧化”或“还原”)。
参考答案:(12分)
 本题解析:略
本题解析:略
本题难度:简单
2、选择题 2008年北京奥运会所用火炬燃料为丙烷,悉尼奥运会所用火炬燃料为65%丁烷和35%丙烷。已知丙烷的燃烧热为:2221.5kJ・mol-1,正丁烷的燃烧热为:2878kJ・mol-1,异丁烷的燃烧热为:2869.6kJ・mol-1。下列有关说法不正确的是
A.奥运火炬燃烧时的能量转化主要是化学能转变为热能
B.丙烷燃烧的热化学方程式为:C3H8+5O2==3CO2+4H2O△H=-2221.5kJ・mol-1
C.相同物质的量的正丁烷和丙烷分别完全燃烧,前者需要的氧气多,产生的热量也多
D.异丁烷比正丁烷稳定
参考答案:B
本题解析:略
本题难度:一般
3、选择题 在同温同压下,下列各组热化学方程式中ΔH1>ΔH2的是?? ( )。
A.2H2(g)+O2(g)=2H2O(l) ΔH1;2H2(g)+O2(g)=2H2O(g) ΔH2
B.S(g)+O2(g)=2SO2(g) ΔH1;S(s)+O2(g)=2SO2(g) ΔH2
C.C(s)+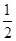 O2(g)=CO(g) ΔH1;C(s)+O2(g)=CO2(g) ΔH2
O2(g)=CO(g) ΔH1;C(s)+O2(g)=CO2(g) ΔH2
D.H2(g)+Cl2(g)=2HCl(g) ΔH1;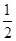 H2(g)+
H2(g)+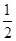 Cl2(g)=HCl(g) ΔH2
Cl2(g)=HCl(g) ΔH2
参考答案:C
本题解析:A项中生成液态水比生成气态水放出的热量多,故ΔH1<ΔH2;B项中气态硫参加反应时比固态硫放出的热量多,则ΔH1<ΔH2;C项中生成CO时比生成CO2放出的热量少,ΔH1>ΔH2;D项中ΔH1=2ΔH2<0,即ΔH1<ΔH2。
本题难度:简单
4、选择题 下列说法或表示方法正确的是???????????(???)
A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ・mol-1可知,若将含1 mol CH3COOH的稀溶液与含1 mol NaOH的稀溶液混合,放出的热量小于57.3 kJ
C.300℃、30MPa下,将0.5molN2(g)和1.5mol H2(g)置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g) △H=-38.6kJ・mol-1
2NH3(g) △H=-38.6kJ・mol-1
D.由C(石墨)=C(金刚石)△H=" +1.90" kJ・mol-1可知,金刚石比石墨稳定
参考答案:B
本题解析:
试题分析:气态S的能量高于固态S的能量,所以等物质的量的硫蒸气和硫固体分别完全燃烧,前者放出热量多,A不正确;醋酸是弱酸,溶于水存在电离平衡,而电离是吸热的,则将含1 mol CH3COOH的稀溶液与含1 mol NaOH的稀溶液混合,放出的热量小于57.3 kJ,选项B正确;选项C中的反应是可逆反应,则不能计算该反应的反应热,C不正确;选项D中石墨的总能量低于金刚石的总能量。能量越低越稳定,所以石墨比金刚石稳定性强,D不正确,答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题。试
本题难度:简单
5、选择题 已知 (1)? H2(g)+1/2O2(g)=H2O(g)????△H1=a kJ/mol
(2)2H2(g)+O2(g)=2H2O(g)?????△H2=b kJ/mol
(3)H2(g)+1/2O2(g)=H2O(l)?????△H3=c kJ/mol
(4)2H2(g)+O2(g)=2H2O(l)??????△H4=d kJ/mol
下列关系式中正确的是???(????)
A.a<c<0
B.b>d>0
C.2a=b<0
D.2c=d>0
参考答案:C
本题解析:氢气燃烧是放热反应,△H小于0。由于气态水的能量高于液态水的能量,所以氢气燃烧生成液态水放出的能量多,但放热越多,反应热越小,所以选项C正确,其余都是错误的,答案选C。
本题难度:简单