微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 用仪器A、B和胶管组成装置收集NO气体(①仪器A已经气密性检查;②除水外不能选用其他试剂)。

正确的操作步骤是:________________________________________。
2、实验题 (20分)现用质量分数为98%.密度为1.84 g/ml的浓硫酸来配制500ml0.2mol/l的稀硫酸,可供选择的仪器如下;①玻璃棒②烧瓶③烧杯④胶头滴管⑤量筒⑥容量瓶⑦托盘天平⑧药匙请回答下列问题。
(1)上述仪器中,在配制稀硫酸时用不到的仪器有??????????????(填序号)
(2)经计算,需浓硫酸的体积为?????????????。现有①10ml.②50ml.③100ml三种规格的量筒,你选用的量筒是??????????(填序号)
(3)将浓硫酸稀释后,冷却片刻,随后全部转移到???????ml的容量瓶中,转移时应用玻璃棒???????,转移完毕后,用少量蒸馏水洗涤烧杯玻璃棒2~3次,并将洗涤液也转入容量瓶中,在加适量蒸馏水直到液面接近刻线???????处。改用????????滴加蒸馏水到瓶颈刻度的地方,将溶液振荡,摇匀后,装瓶,贴签。
(4)下列情况对所配制的稀硫酸浓度有何影响?(用偏高、偏低、无影响填写)
A、容量瓶用蒸馏水洗涤后未干燥_________________;
B、所用的浓硫酸长时间放置在敞口容器内_________________;
C、定容时仰视溶液的凹液面_________________;
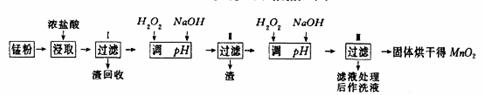
3、填空题 (16分)回收的废旧锌锰干电池经过处理后可得到锰粉(主要含MnO2、Mn(OH)2、Fe、NH4Cl和炭黑等),由锰粉制取MnO2的步骤和数据如下:
物质
| 开始沉淀
| 沉淀完全
|
Fe(OH)3
| 2.7
| 3.7
|
Fe(OH)2
| 7.6
| 9.6
|
Fe(OH)2
| 8.3
| 9.8
??(1)在加热条件下,用浓盐酸浸取锰粉得到含有Mn2+、Fe3+等离子的溶液,MnO2与浓盐酸反应的离子方程式?????????,该处理方法的缺点?????????。
(2)步骤I中滤渣的化学式?????????,步骤I中滤渣的化学式?????????。
(3)向步骤I的滤液中加足量H2O2的作用为?????????。再加NaOH溶液调节pH在3.7<pH<8.3,目的是???????????????????。
(4)向步骤II的滤液中H2O2溶液,再加NaOH溶液调节pH为9,使Mn2+转化成MnO2,在这一过程中H2O2起?????????(填氧化剂、还原剂)的作用。
4、填空题 在实验室我们也可以用下图所示的装置制取乙酸乙酯。

(1)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的方法是????。
(2)写出制取乙酸乙酯的化学方程式??????????????????。
(3)饱和碳酸钠溶液的主要作用除了吸收乙酸和乙醇外,还有????????????。
(4)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,其目的是????????。
(5)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是??????????。
5、选择题 下列关于实验室制取氯气的操作正确(??? )
①用药匙向烧瓶中加入浓盐酸,再向分液漏斗中装入MnO2粉末;
②用酒精灯直接加热烧瓶;
③需检查装置的气密性;
④多余氯气用NaOH溶液吸收;
⑤可用装有碱石灰的干燥管干燥氯气。
A.①④⑤
B.③④
C.②④⑤
D.①②③
|