微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 金属单质A与盐酸反应生成浅绿色溶液B,同时放出气体C。如果在B溶液中通入氯气,则B转变成棕黄色溶液D,将溶液D分为两份,一份加入几滴KSCN溶液,溶液变成血红色,另一份加入A,则棕黄色溶液D重新变成浅绿色溶液B。则:
(1)各物质的化学式分别是:A________ ,B________ ,C________ ,D________;
(2)有关反应的离子方程式有:
① B→D___________________________;
② D→B____________________________。
参考答案:(1)Fe?? FeCl2? H2? FeCl3
(2
本题解析:
试题分析:氯化亚铁溶液呈浅绿色,氯化铁溶液呈棕黄色,前者可被氯气氧化为后者,氯化铁遇KSCN溶液变红,氯化铁溶液被铁还原为氯化亚铁,铁与盐酸反应生成氯化亚铁和氢气,由此推断A、B、C、D分别为Fe、FeCl2、H2、FeCl3;根据离子方程式和氧化还原反应方程式的配平可知,B→D的反应式为2Fe2++Cl2=2Fe3++Cl―;D→B的反应式为2Fe3++Fe=3Fe2+。
本题难度:简单
2、填空题 (14分)某混合物X由A12O3、Fe2O3、Cu、SiO2中的一种或几种物质组成。进行如下实验。

请回答:
(1)由I可知X中一定存在的是????????????,步骤I所发生反应的离子方程式为:?????????????????????????、???????????????????????????。
(2)反应II的化学方程式是????????????????? ??????????????。
为进一步确定上述混合物X的成分,另取9.4gX进行如下实验。

(3)由Ⅲ可得出的结论为:??????????????????????????????????????????。
(4)步骤Ⅳ所得蓝色溶液中阳离子为????????????????。
(5)原混合物中各成分的质量之比是????????????????。(不必化简)
参考答案:(1)Fe2O3、Cu???? Fe2O3+6H+===2F
本题解析:(1)和过量的盐酸反应所得溶液显蓝色,说明有铜离子生成。由于单质铜和盐酸是不反应的,所以必须含有氧化铁,氧化铁和盐酸反应生成的铁离子能氧化单质铜,因此X中一定存在的是Fe2O3、Cu,步骤I所发生反应的离子方程式为Fe2O3+6H+===2Fe3++3H2O、? Cu+2Fe3+===2Fe2++Cu2+。
(2)由于剩余的固体和氢氧化钠反应后,仍然有固体剩余,这说明4.92g固体中一定含有二氧化硅,和氢氧化钠溶液的方程式是SiO2+2NaOH===Na2SiO3+H2O。
(3)根据(2)可
本题难度:一般
3、选择题 下列叙述I和II均正确并且有因果关系的是
选项
| 陈述I
| 陈述II
|
A
| NH4Cl为强酸弱碱盐
| 用加热法除去NaCl中的NH4Cl
|
B
| Fe3+具有氧化性
| 用KSCN溶液可以鉴别Fe3+
|
C
| 溶解度:CaCO3<Ca(HCO3)2
| 溶解度:Na2CO3<NaHCO3
|
D
| SiO2可与HF反应
| 氢氟酸不能保存在玻璃瓶中
参考答案:D
本题解析:NH4Cl为强酸弱碱盐的原因是HCl是强酸、NH3?H2O是弱碱,用加热法除去NaCl中的NH4Cl的原因是NH4Cl受热易分解为氨气、氯化氢气体,而NaCl的热稳定性很强,则陈述I、II均正确,但是它们没有因果关系,A项错误;Fe3+具有氧化性的原因是铁元素的化合价可以从+3价将为+2价甚至0价,用KSCN溶液可以鉴别Fe3+的原因是Fe3+遇KSCN溶液迅速显红色,则陈述I、II均正确,但是它们没有因果关系,B项错误;向碳酸钙悬浊液中通入过量二氧化碳气体可得澄清溶液,说明碳酸钙是难溶于水的钙盐,碳酸氢
本题难度:一般
4、实验题 某小组同学设计实验探究Fe3+与Fe2+相互转化,实验方案及现象如下:
Ⅰ. 配制FeCl2溶液
取部分变质的氯化亚铁固体[含有难溶性杂质Fe(OH)2Cl],向其中加入稀盐酸,使其完全溶解,再加入适量铁粉。
Ⅱ. 实验探究Fe3+与Fe2+相互转化
实验1:
0.1 mol/L FeCl2溶液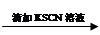 无明显现象 无明显现象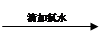 溶液变红 溶液变红
实验2:
0.1 mol/L FeCl3溶液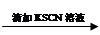 溶液变红 溶液变红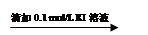 溶液红色未褪去 溶液红色未褪去
写出Fe(OH)2Cl与盐酸反应的离子方程式???????。
(2)请用离子方程式解释实验1中滴加氯水后溶液变红的原因??????。
(3)实验2的现象与预测不同, 为探究可能的原因,该小组同学又进行了如下实验,方案及现象如下:
步骤1:10 mL 0.1 mol/L KI溶液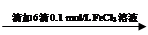 溶液明显变黄 溶液明显变黄
步骤2:将黄色溶液分为三份:
试管1 取2 mL黄色溶液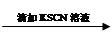 溶液变红 溶液变红
试管2 取3 mL黄色溶液 溶液变蓝 溶液变蓝
试管3 取3 mL黄色溶液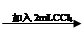 取上层溶液 取上层溶液 溶液变蓝(比试管2中溶液颜色深) 溶液变蓝(比试管2中溶液颜色深)
① 试管2中滴加K3[Fe(CN)6]检验的离子是???????。
② 黄色溶液中含有的溶质微粒有K+、Cl-和???????。
③ 综合上述实验现象,得出的实验结论是???????。
参考答案:
(1)Fe(OH)2Cl + 2H+ = Fe3+
本题解析:
试题分析:
(1)根据题意可得:Fe(OH)2Cl + 2H+ = Fe3+ + Cl- + 2H2O
(2)Cl2 与Fe2+发生氧化还原反应:2Fe2+ + Cl2 = 2Cl- + 2Fe3+(1分)
(3)①K3[Fe(CN)6]专门用于检验的Fe2+试剂;?②滴加KSCN溶液溶液变红有Fe3+、加2滴K3[Fe(CN)6]溶液溶液变蓝有Fe2+、滴加6滴0.1 mol/L FeCl3溶液溶液明显变黄有I2?;③反应物、生成物都存在,试管3中实验说明平衡移动,则Fe3+与
本题难度:一般
5、选择题 今有3mol・L-1盐酸和硫酸溶液各100mL,分别加入等质量的铁粉,反应完毕后,生成气体的质量比为3∶4,则盐酸中加入铁粉的质量为 (??)
A.5.6g
B.8.4g
C.11.2g
D.16.8g
参考答案:C
本题解析:略
本题难度:一般
|