微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (17分)中学化学常见的滴定法包括中和滴定法、氧化还原反应滴定法等。
(1)探究小组甲用酸性KMnO4溶液滴定某补血剂[主要成分硫酸亚铁晶体(FeSO4?7H2O)]中铁元素的含量。
①下列滴定装置中(夹持部分略去),最合理的是: (填字母序号)。

②实验前,首先要准确配制一定物质的量浓度的酸性KMnO4溶液250mL,配制时需要的仪器除托盘天平、玻璃棒、烧杯、胶头滴管、量筒外,还需要 (填仪器名称)。
③该小组拟在同浓度的FeSO4溶液中,探究酸性KMnO4溶液浓度对Fe2+被氧化时反应速率的影响。限选试剂与仪器:0.10mol?L-1FeSO4、0.02mol?L-1酸性KMnO4、蒸馏水、锥形瓶、试管、胶头滴管、量筒、秒表。参照下表格式,完成实验表格(列出所选试剂体积和数据;数据用字母表示)。
 物理量 物理量
实验序号
| V[0.10mol?L-1FeSO4]
/mL
|
|
| KMnO4溶液褪色所需时间t/s
|
1
| a
|
|
| t1
|
2
| a
|
|
| t2
(2)常温下,探究小组乙将0.1 mol・L-1盐酸滴入20 mL 0.1 mol・L-1氨水中,溶液的pH随加入盐酸体积的变化曲线如右图所示。
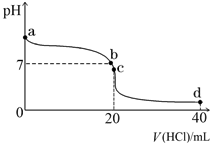
①a点处假设溶液的pH=10,则该点处由水电离产生的c(OH-)= 。
②b点处溶液中c (Cl-) c (NH4+)(填“>”、“<”或“=”)。
③取c点时的饱和溶液并向其加入水玻璃(硅酸钠水溶液),振荡、静置。写出实验现象并用必要的文字和相关离子方程式给予解释: 。
④d点所示溶液中离子浓度由大到小的排序是 。
2、填空题 X、Y、Z三种短周期元素,其中X元素的原子序数大于Y,且X、Y的氧化物都是形成酸雨的主要物质。Z是地壳中含量最高的金属元素;而地壳中含量最高的非金属元素与X同主族、与Y同周期。
(1)实验室用H2XO4制取XO2气体的化学反应方程式为 。(请用具体元素符号表示化学式,下同)
(2)t℃时,0.1 mol・L-1的NaHXO3溶液pH=6,该溶液中各离子浓度由大到小顺序排列为 。
(3)请写出Z的氧化物与烧碱溶液反应的离子方程式 。
(4)一定条件下,YO与YO2存在下列反应:YO(g)+ YO2(g)  Y2O3(g),其平衡常数表达式为K= 。 Y2O3(g),其平衡常数表达式为K= 。
(5)工业上用氧化YH3法制取YO,该反应的热化学方程式为:
4YH3(g)+5O2(g)=4YO(g)+6H2O(g) △H=-905.8kJ・mol-1;
已知Y2(g)+O2(g)=2YO(g) △H="+180" kJ・mol-1,则YH3与氧气反应产生两种无污染物质的热化学式为 。
3、选择题 0.1 mol・L-1的某溶液的pH=5.1,此溶液可能是
①NaCl
②CH3COONa
③HCl
④NH4Cl
A.①②
B.③④
C.②③
D.④
4、选择题 已知:某元素X的酸式盐(NaHX)溶液显碱性,下列说法正确的是
A.NaHX的电离方程式为NaHX===Na+ + H+ + X2¯
B.HX¯的电离程度小于HX¯的水解程度
C.离子浓度关系:c(Na+) + c(H+) = c(OH¯) + c(HX¯) + c(X2¯)
D.加水稀释,促进HX¯水解,c(HX¯)增大
5、选择题 将pH=3的盐酸溶液和pH=11的氨水等体积混合后,溶液中离子浓度关系正确的是:( )
A.c(NH4+)>c(Cl
|