微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 金属及其化合物在生产、生活中有广泛应用.请回答下列问题:
(1)工业上常利用Fe2+能与CN-形成稳定Fe(CN)4-6(六氰合亚铁离子)的特点来处理含CN-的工业废水.
①写出基态Fe2+的电子排布式______.
②从结构角度分析Fe3+较Fe2+稳定的原因______.
③CN-中C原子的杂化轨道类型为______.
(2)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华.易溶于水,也易溶于乙醚、丙酮等有机溶剂.据此判断三氯化铁晶体中存在的微粒间作用力有______.
(3)铁元素为血红蛋白和肌红蛋白的活性部分--血红素的重要组成部分;
①血红素的结构式为:
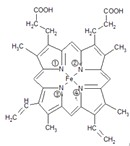
血红素中含有C、H、O、N、Fe五种元素,C、N、O三种元素的第一电离能由小到大的顺序是______.铁原子周围哪些氮原子参与形成了配位键______(空格上填氮原子标号).
(4)钙是人体所需的重要元素之一,有一种补钙剂--抗坏血酸钙的组成为Ca(C6H7O6)2?4H2O,其结构示意图如下:
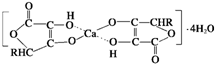
该物质中存在的化学键类型包括______(填字母).
A.金属键B.离子键 C.非极性共价键D.配位键
(5)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是______.
2、填空题 水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
(1)氧原子在基态时,核外电子的轨道表示式为__________。
(2)写出与H2O分子互为等电子体的两种微粒_____________。
(3)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是
__________。
a.氧原子的杂化类型发生了改变
b.微粒的形状发生了改变
c.微粒的化学性质发生了改变
d.微粒中的键角发生了改变
(4)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排列)。与冰的晶体类型相同的是
________ (请用相应的编号填写)。
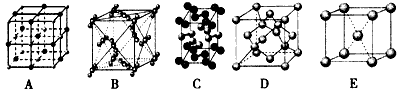
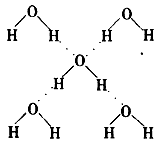
(5)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示)。已知冰的升华热是51 kJ/mol,除氢键外,水分子间还存在范德华力(11 kJ/mol),则冰晶体中氢键的“键能”是___________kJ/mol。
(6)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子。生成此配合离子的离子方程式为____________。
3、选择题 下列各组中的物质或离子都含配位键的是( )
A.H2O、Al2Cl6
B.CO2、SO42-
C.PCl5、[Co(NH3)4Cl2]Cl
D.NH4Cl、[Cu(NH3)4]SO4
4、选择题 下列关于各配合物的稳定性,判断不正确的是[???? ]
A.[Fe(CN)6]3->[Fe(SCN)6]3-
B.[HgCl4]2->[HgF4]2-
C.[AlF6]3->[AdBr6]3-
D.[Cu(NH3)4]2+>[Zn(NH3)4]2+
5、选择题 某物质的实验式为PtCl4?2NH3,其水溶液不导电,加入AgNO3溶液反应也不产生沉淀,以强碱处理并没有NH3放出,则关于此化合物的说法中正确的是( )
A.配合物中中心原子的电荷数和配位数均为6
B.该配合物可能是平面正方形结构
C.Cl-?和NH3分子均与Pt4+配位
D.配合物中Cl-?与Pt4+配位,而NH3分子不配位