微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在-50 ℃时液氨中有2NH3(液)  NH4++NH2―电离平衡关系,两离子的平衡浓度均为1×10-15mol・L-1,下列对-50 ℃时液氨的电离平衡常数的表达中正确的是
NH4++NH2―电离平衡关系,两离子的平衡浓度均为1×10-15mol・L-1,下列对-50 ℃时液氨的电离平衡常数的表达中正确的是
A.电离平衡常数是1×10-15
B.不加入其他物质,液氨中c(NH4+)=c(NH2―)
C.降低温度,其电离平衡常数数值增加
D.此液氨中放入NH4Cl,其电离平衡常数的数值增加
2、选择题 一元弱酸HA(aq)中存在下列电离平衡:HA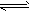 A-+H+。将1.0 mol HA分子加入1.0 L水中,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是 [???? ]
A-+H+。将1.0 mol HA分子加入1.0 L水中,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是 [???? ]
A.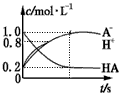
B.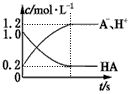
C.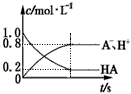
D.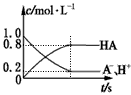
3、选择题 已知在常温下测得浓度均为0.1mol/L的下列6种溶液的pH值:
溶质
| CH3COONa
| NaHCO3
| Na2CO3
| NaClO
| NaCN
| C6H5ONa
|
pH
| 8.8
| 9.7
| 11.6
| 10.3
| 11.1
| 11.3
?
下列说法或表达中,正确的是
A.少量二氧化碳通入NaClO溶液中:2NaClO + CO2 + H2O Na2CO3 + 2HClO Na2CO3 + 2HClO
B.过量的HCN滴入碳酸钠溶液中HCN + Na2CO3 NaCN+ NaHCO3 NaCN+ NaHCO3
C.结合质子能力由强到弱的顺序为:CO32―>CN―>HCO3―>CH3COO―
D.常温下电离常数:Ki2(H2CO3)>Ki(C6H5OH)>Ki(HCN)
4、选择题 将0.01 mol的下列物质分别加入(或通入)到100mL水中,假设溶液体积变化不计,水溶液的导电能力最强的是(?? )
A.HF
B.NH4HCO3
C.BaSO4
D.NH3
5、选择题 在0.1mol/L的H2S溶液中,下列关系错误的是(?)
A.c(H+)=c(HS-)+c(S2-)+c(OH-)
B.c(H+)=c(HS-)+2c(S2-)+c(OH-)
C.c(H+)>[c(HS-)+c(S2-)+c(OH-)]
D.c(H2S)+c(HS-)+c(S2-)="0.1mol/L"
|