微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将镁、铝、锌、铁四种金属分别与足量的稀盐酸反应,图中各曲线表示的是消耗金属的质量 与产生氢气的质量
与产生氢气的质量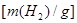 之间的关系,其中能代表
之间的关系,其中能代表 质量关系的是
质量关系的是
参考答案:C
本题解析:镁、铝、锌、铁四种金属与盐酸反应,均失去1mol电子得到等量的氢气时,各金属的质量分别为12g、9g、32.5g、28g,对比图示可知,ABCD四线分别代表铝、镁、铁、锌,故答案为C
本题难度:一般
2、选择题 等质量的钠进行下列实验,最终生成氢气最多的是(??)
A.将钠投入到足量水中
B.将钠用铝箔包好并刺一些小孔,再投入足量水中
C.将钠投入足量稀硫酸中
D.将钠投入足量饱和食盐水中
参考答案:B
本题解析:
试题分析:如果钠的质量相等,则不论是和水反应,还是和酸反应,生成的氢气都是相等的。但选项B中铝箔还能和生成的氢氧化钠溶液反应生成氢气,所以选项B生成的氢气最多,答案选B。
点评:铝是活泼的金属,但铝还能和强碱溶液反应生成氢气,搞清楚这一点,该题就不难得出答案。
本题难度:一般
3、填空题 一定质量的液态化合物XY2,在标准状况下的一定质量的O2中恰好完全燃烧,反应方程式为:XY2(l)+3O2(g)===XO2(g)+2YO2(g),冷却后,在标准状况下测得生成物的体积是672 mL,密度是2.56 g/L,则:
(1)反应前O2的体积是________________。
(2)化合物XY2的摩尔质量是________________。
(3)若XY2分子中X、Y两元素的质量比是3∶16,则X、Y两元素分别为________和__________(写元素符号)。请写出 Y的离子结构示意图为???????????????????。
(4)已知X元素有aX、bX、cX三种原子,Y元素有eY、f Y 两种原子,则它们能够形成??????种XY2分子。
参考答案:(1)672mL。? (2)76g/mol。????(3)
本题解析:(1)根据反应的方程式可知,反应前后体积是不变的,所以反应前氧气的体积是672ml。
(2)标准状况下,672ml气体的物质的量是0.672L÷22.4L/mol=0.03mol。即参加反应的氧气是0.03mol,化合物XY2的物质的量是0.01mol。标准状况下的密度是2.56 g/L,则混合气的质量是2.56 g/L×0.672L。根据质量守恒定律可知,0.01×M+0.03×32=2.56 ×0.672,解得M=76,所以化合物XY2的摩尔质量是76g/mol。
(3)设X的相对原子质量
本题难度:一般
4、计算题 有一种氯化钠与氯化钾的混合物,它所含钾与钠的物质的量之比为3∶1。求:
(1)混合物中氯化钾的质量分数。
(2)含1 mol Cl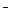 的该混合物的质量。
的该混合物的质量。
参考答案:(1)79.3%? (2)70.5 g
本题解析:(1)NaCl与KCl的物质的量之比等于Na与K的物质的量之比。
则n(NaCl)∶n(KCl)=1∶3。
设NaCl为1 mol,则KCl为3 mol。
则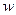 (KCl)=
(KCl)= 本题难度:简单
本题难度:简单
5、选择题 NA表示阿伏加德罗常数的值,下列叙述正确的是
A.5.6 g铁与足量硫的反应中,铁失去的电子数为0.3NA
B.标准状况下,22.4 L SO3所含原子数为4 NA
C.1.8g的NH4+离子中含有的电子数为NA
D.20 g D2O中所含的中子数为8 NA、
参考答案:C
本题解析:略
本题难度:简单