微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (14分)锰锌铁氧体可制备隐形飞机上吸收雷达波的涂料。以废旧锌锰电池为原料制备锰锌铁氧体(MnxZn1-xFe2O4)的主要流程如下,请回答下列问题:

(1)酸浸时,二氧化锰被双氧水还原的化学方程式为 。
(2)活性铁粉除汞时,铁粉的作用是 (填“氧化剂”或“还原剂”或“吸附剂”)。
(3)除汞是以氮气为载气吹入滤液中,带出汞蒸汽经KMnO4溶液进行吸收而实现的。下图是KMnO4溶液处于不同pH时对应Hg的单位时间去除率变化图,图中物质为Hg与 MnO4-在该pH范围内反应的主要产物。
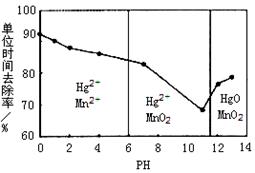
①pH<6时反应的离子方程式为 。
②请根据该图给出pH对汞去除率影响的变化规律: 。
③试猜想在强酸性环境下汞的单位时间去除率高的原因: 。(不考虑KMnO4在酸性条件下氧化性增强的因素)
(4)当x=0.2时,所得到的锰锌铁氧体对雷达波的吸收能力特别强,试用氧化物的形式表示该锰锌铁氧体的组成 。
(5)经测定滤液成分后,需加入一定量的MnSO4和铁粉,其目的是 。
参考答案:(14分)
(1)MnO2 + H2O2&#
本题解析:
试题分析:(1)酸浸时,二氧化锰作氧化剂,过氧化氢作还原剂,则过氧化氢被氧化为氧气,则二氧化锰被还原为锰离子,所以发生的化学方程式是MnO2 + H2O2 + H2SO4=MnSO4 +O2↑ + 2H2O;
(2)铁粉与汞离子发生置换反应生成亚铁离子和单质汞,所以加入的铁粉在该反应中作还原剂;
(3)①pH<6时,以锰离子和汞离子形式存在,则Hg被高锰酸钾溶液吸收,生成锰离子和汞离子,因为是酸性溶液,所以有氢离子参加,产物中有水生成,离子方程式是5Hg+2MnO4-+16H+=5Hg2++2Mn2++8H2O;
②根据图像中曲线的走势可判断,随pH的升高汞的去除率先降低后增加;
③不考虑KMnO4在酸性条件下氧化性增强的因素,反应开始产生的锰离子对该反应具有催化作用,使反应速率加快,单位时间去除率高;
(4)x=0.2时,+2价Mn与+2价Zn的个数比是0.2:0.8=1:4,Mn、Zn整体与+3价Fe的比是1:2,所以该锰锌铁氧体的组成可表示为MnO・4ZnO・5Fe2O3;
(5)根据(4)可知锰锌铁氧体物质中各金属元素原子应满足一定的个数比,所以加入硫酸锰和Fe粉的目的是调节滤液离子的成分,符合水热后获得锰锌铁氧化体组成。
考点:考查对物质制备流程的分析与判断
本题难度:困难
2、选择题 已知25 ℃时,下列酸的电离常数:醋酸:1.75×10-5氢氰酸:4.93×10-10
氢氟酸:7.2×10-4甲酸:1.77×10-4则物质的量浓度均为0.1 mol・L-1的上述溶液酸性最强的是 ( )
A 醋酸 B 氢氰酸 C氢氟酸 D甲酸
参考答案:C
本题解析:
正确答案:C
浓度相同时,组成相似的酸,电离常数越大,酸性越强,氢氟酸:7.2×10-4,酸性最强。
本题难度:简单
3、填空题 已知水在25?℃和95?℃时,其电离平衡曲线如图所示
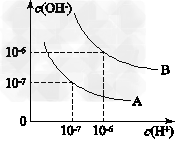
(1)则25?℃时水的电离平衡曲线应为________(填“A”或“B”),请说明理由_________________________________________________。
(2)25?℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为________。
(3)95?℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,pH1与pH2之间应满足的关系是________。
(4)曲线B对应温度下,pH=2的某HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5。请分析其原因___________________________。
参考答案:(1)A;水的电离是吸热过程,温度低时,电离程度小,c(H+
本题解析:
本题难度:一般
4、实验题 (7分)用中和滴定法测定烧碱的纯度,若烧碱中含有与酸不反应的杂质,试根据实验回答:
(1)将准确称取的4.3 g烧碱样品配制成250 mL待测液,需要的主要仪器除量筒、烧杯、玻璃棒、胶头滴管外,还必须用到的仪器有 。
(2)取待测液10.00 mL,用 滴定管量取,并置于锥形瓶中。
(3)向锥形瓶中滴加几滴指示剂,用0.200 mol・L-1标准盐酸滴定待测烧碱溶液。不适宜选用的指示剂为(选填序号):________。①石蕊试液 ②无色酚酞 ③甲基橙试液
(4)根据两次滴定获得的实验数据如下表,得出烧碱的纯度为 。
滴定次数
| 待测液体积(mL)
| 标准盐酸体积(mL)
|
滴定前读数(mL)
| 滴定后读数(mL)
|
第一次
| 10.00
| 0.50
| 20.40
|
第二次
| 10.00
| 4.00
| 24.10
(5)下列操作中可能使所测烧碱溶液的浓度数值偏低的是(选填字母) 。
A 酸式滴定管未用盐酸标准溶液润洗就直接注入盐酸标准溶液
B 锥形瓶用蒸馏水洗净后没有干燥就注入NaOH待测液
C 装有盐酸标准溶液的酸式滴定管在滴定前有气泡,滴定后气泡消失
D 读取HCl溶液体积时,开始仰视读数,滴定结束时俯视读数
E.若刚见到指示剂局部的颜色有变化就停止滴定
参考答案:(1)250 mL容量瓶(1分);(2)碱式(1分);(3)
本题解析:
试题分析:(1)配制步骤有计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,冷却后转移到250mL容 量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、250mL容量瓶、 胶头滴管,缺少250mL容量瓶。
(2)待测液是碱性溶液,应盛放在碱式滴定管中。
(3)石蕊试液颜色变化不明显,滴定终点较难判断,所以不宜选用的指示剂为石蕊试液。
(4)V(标准)
本题难度:一般
5、填空题 (10分)某温度(t℃)时,水的离子积为KW=1×10-13,则该温度(填“大于”、“小于”或“等于”)________25℃。若将此温度下pH=11的苛性钠溶液a L与pH=1的稀硫酸b L混合(设混合后溶液体积的微小变化忽略不计),试通过计算填写以下不同情况时两种溶液的体积比:
①若所得混合液为中性,则a∶b=________;此溶液中各种离子的浓度由大到小排列顺序是________________ 。
②若所得混合液的pH=2,则a∶b=________。此溶液中各种离子的浓度由大到小排列顺序是_______ _。
参考答案:
大于;①10:1;c(Na+)>c(SO42-
本题解析:略
本题难度:一般
|