微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 完成下列计算
(1) 相同物质的量的O2和O3的质量比____,分子个数比为______,所含氧原子的个数比为_______.
(2) 在200 mL 2 mol/L MgCl2溶液中,溶质的质量为________.此溶液中Mg2+的物质的量浓度为___________,Cl-的物质的量浓度为________.
(3) 在质量分数为28%的KOH水溶液中,OH-与H2O数目之比是________.
参考答案:(1)2:3, 1:1 ,2:3(2
本题解析:
试题分析:(1)根据m=nM可知,相同物质的量的O2和O3的质量之比=32g/mol:48g/mol=2:3,由N=nN可知,分子数目之比等于物质的量之比=1:1;氧气所含氧原子数目为氧气分子2倍,臭氧所含氧原子数目为臭氧分子的3倍,故相同物质的量的O2和O3含有氧原子数目之比=1×2:1×3=2:3,故答案为:2:3;1:1;2:3;(2)200mL 2mol?L-1MgCl2溶液中,氯化镁的物质的量为:2mol?L-1×0.2L=0.4mol,氯化镁的质为:95g/mol×0.4mol=38g,此溶液中Mg2+的物质的量浓度为:c(Mg2+)=c(MgCl2)=2mol?L-1, 此溶液中Cl-的物质的量浓度为:c(Cl-)=2c(MgCl2)=4mol?L-1,故答案为:38g;2mol?L-1;4mol?L-1.(3)假设溶液质量为100g,则KOH的质量=100g×28%=28g,故水的质量=100g-28g=72g,故KOH的物质的量=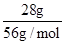 =0.5mol、水的物质的量=
=0.5mol、水的物质的量=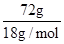 =4mol,故溶液中OH-与H2O数目之比=0.5mol:4mol=1:8
=4mol,故溶液中OH-与H2O数目之比=0.5mol:4mol=1:8
考点:物质的量的相关计算
本题难度:一般
2、填空题 (1).经科学测定,人体平均含氧65%,含碳18%,含氢10%(均以质量计),则三种元素中原子数目最多的是______.
(2).Al2(SO4)3的摩尔质量是______,在6.84g?Al2(SO4)3固体中,n(Al3+)=______.将上述一定量的硫酸铝溶于水后,再加入足量的BaCl2溶液使之完全反应,消耗BaCl2的物质的量______.
参考答案:(1)设人体的质量为m,则人体中该元素原子的物质的量=m×质
本题解析:
本题难度:简单
3、计算题 已知8g A能与32g B恰好完全反应,生成22g C和一 定量D,现将16g A与200g B的混合物充分反应后,生成 2mol D和一定量C,则D的摩尔质量为多少?
参考答案:一个化学反应的进行必须遵循质量守恒定律,根据题中第一个条件,
本题解析:
本题难度:一般
4、选择题 某盐的混合物中含有0.1mol Na+、0.6mol Mg2+、0.3mol Cl-,还有SO42-,则SO42-为
A.0.1mol
B.0.5mol
C.0.3 mol
D.0.7mol
参考答案:B
本题解析:
试题分析:根据电荷守恒,溶液中阳离子所带正电荷等于阴离子所带负电荷。
本题难度:一般
5、选择题 下列各溶液中,Na+浓度最大的是( )
A.4L 0.5mol/L NaCl溶液
B.1L 0.3mol/L Na2SO4溶液
C.0.8L 0.4mol/L NaOH溶液
D.2L 0.15mol/L Na3PO4溶液
参考答案:A、4L0.5mol/LNaCl溶液中Na+浓度为0.5mo
本题解析:
本题难度:一般