微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列离子方程式正确的是(??? )
A.二氧化硫通入足量KOH溶液中SO2+2OH-
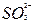 +H2O
+H2O
B.往澄清石灰水中通入足量二氧化硫SO2+Ca2++2OH- CaSO3↓+H2O
CaSO3↓+H2O
C.往二氧化硫的水溶液中滴加少量NaOH溶液H2SO3+OH-
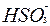 +H2O
+H2O
D.亚硫酸中滴加双氧水生成硫酸H2SO3+2H++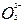
 2H++
2H++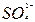 +2H2O
+2H2O
参考答案:AC
本题解析:B项中应生成HSO-3,D项中双氧水应写成分子式。
本题难度:简单
2、实验题 (18分)I.实验室制备、收集干燥的SO2,所需仪器如下。

(1)装置A产生SO2,按气流方向连接各仪器接口,顺序为a→ ____→ ____ →____→____f。
(2)装置A中发生反应的化学方程式为____________________________________。
(3)验证产生的气体是SO2的方法是________________________________________。
II.SO2气体为无色气体,有强烈刺激性气味,大气主要污染物之一,具有一定的还原性,探究SO2气体还原Fe3+、I2可以使用的药品和装置如图所示:
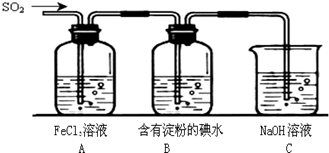
(1)装置A中的现象是__________。在SO2还原Fe3+的反应中SO2和Fe3+的物质的量之比是_______。
(2)装置C的作用是____________________________________。
(3)若要从A中的FeCl3溶液中提取晶体,必须进行的实验操作步骤:加热浓缩、冷却结晶、过滤,在这一系列操作中没有用到的玻璃仪器有(? )
A.烧瓶
B.酒精灯
C.漏斗
D.烧杯 E.玻璃棒
(4)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,取A中的溶液,分成两份,并设计了如下实验:
方案①:往第一份试液中加入少量酸性KMnO4溶液,紫红色褪去。
方案②:往第二份试液中加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
上述方案不合理的是______,原因是___________________________________。
(5)能表明的还原性性弱于SO2的现象是________________________________________。
参考答案:I.(1)d→e→c→b (2)Cu+2H2SO4(浓)
本题解析:
试题分析:I.(1)SO2密度比空气大,用向上排空气法收集,收集前需要浓硫酸干燥,最后还需要用氢氧化钠溶液吸收,因此正确的连接顺序为a→d→e→c→b→f。
(2)浓硫酸具有强氧化性,在加热的条件下与铜发生氧化还原反应,反应的化学方程式为Cu+2H2SO4(浓) CuSO4+2H2O+SO2↑。
CuSO4+2H2O+SO2↑。
本题难度:一般
3、选择题 不能鉴别二氧化碳与二氧化硫的试剂是
A.品红溶液
B.澄清的石灰水
C.溴水
D.酸性高锰酸钾溶液
参考答案:B
本题解析:
试题分析:A、SO2可使品红溶液褪色,CO2则不能,故品红可以鉴别SO2和CO2,错误;B、CO2、SO2都是酸性氧化物,都能与澄清石灰水变浑浊,错误;C、CO2不能使溴水褪色,SO2具有还原性,能使溴水褪色,故溴水可以鉴别SO2和CO2,正确;D、CO2不能酸性高锰酸钾溶液褪色,SO2能使酸性高锰酸钾溶液褪色,故可以鉴别SO2和CO2,正确。2的重要化学性质等相关知识。
本题难度:一般
4、选择题 BaCl2有剧毒,致死量为0.8g,万一不慎误服,应大量吞服鸡蛋清来解毒,并加服一定量药剂,此药剂的主要成分是(???)
A.AgNO3
B.Na2SO4
C.Na2CO3
D.MgCl2
参考答案:B
本题解析:BaCl2能引起体内蛋白质的性质改变,引起中毒,可设法使其形成BaSO4沉淀来大大降低毒性。Na2CO3与BaCl2反应生成的BaCO3溶于酸,只有选Na2SO4较妥当。
本题难度:简单
5、填空题
(1)分析判断A和B 各是什么物质,写出各自的化学式。
(2)写出①~⑦各步反应的化学方程式。

参考答案:(1)A、B分别是FeS和FeS2。
(2)①:4Fe
本题解析:本题属于综合推断题。主要考查学生对元素化合物知识掌握的熟练程度及分析、推断能力。
分析判断A和B的方法有很多。
方法一:根据“固体A和B都由两种相同的元素组成。在A、B中两种元素的原子个数比分别为1:1和1:2,可从中学所学的组成关系类似的物质中寻找,以缩小范围。A、B可能是FeS和FeS2。
方法二:根据“A和B煅烧时都生成C(固体)和D(气体)”可知,在学过的物质中只有FeS和FeS2为满足这一条件的化合物。
方法三:从淡黄色沉淀和红褐色沉淀突破:两化合物中含有共同的元素应是硫
本题难度:简单