��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��9�֣�ij�¶ȣ�t ��)ʱ��ˮ�����ӻ�ΪKW =1��10-13,����¶�____ 25 ��(ѡ�������������=��������������________________________________���������¶���pH=11�Ŀ�������Һa L��pH=1��ϡ����b L��ϣ����Ϻ���Һ�����С�仯���Բ��ƣ�����ͨ��������д���²�ͬ���ʱ����Һ������ȡ�
��1�������û����ҺΪ���ԣ���a��b =__________������Һ�и������ӵ�Ũ���ɴ�С������˳����____???????????????������c(Na+)�ȱ�ʾ��
��2�������û��Һ��pH=2����a��b =__________������Һ�и������ӵ�Ũ���ɴ�С������˳����____????????????????������c(Na+)�ȱ�ʾ��
�ο��𰸣�����1�֣�? 25 ��ʱˮ��KW=1��10-1
���������25 ��ʱ��ˮ�����ӻ�ΪKW =1��10-14, KW ��t �棩=1��10-13��KW��25 �棩����ˮ�ĵ��������ȵģ���˵��t��25 �棨���£�ˮ�ĵ���ƽ�������ƶ���KW����
��1�������¶���pH=11�Ŀ�������Һ��C��OH-��="0.01" mol��L��1��
��pH=1��ϡ���ᡱC��H+��="0.1" mol��L��1��
�����û����ҺΪ���ԣ�������ǡ����ȫ��Ӧ������ OH- + H+ = H2O
1?? 1
�����Ѷȣ�һ��
2��ѡ���� ��0.01mol�������ʷֱ����100mL����ˮ�У��ָ������£�������Һ��������Ũ�ȵĴ�С˳���ǣ���Һ����仯���Բ��ƣ�
��Na2O2??????????��Na2O??????????��Na2CO3????????��NaCl
A����>��>��>��
B����>��>��>��
C����=��>��>��
D����=��>��=��
�ο��𰸣�C
�����������
�����Ѷȣ���
3������� ��7�֣���֪��A�����ҺpH=a��B�����ҺpH="b???"
��1����AΪ���ᣬBΪ������������a+b=14�����ߵ������ϣ���Һ��pH=????���������Ϊ1��10��Ϻ���Һ�����ԣ���a+b=????????????��
��2����AΪ���ᣬBΪ�������ƣ���a=4��b=12����ôA��Һ��ˮ�������������Ũ��Ϊ??????????mo1��L�Cl��B��Һ��ˮ�������������Ũ��Ϊ????????????mol��L�C1��
��3����AΪ���ᣬBΪ�������ƣ���a+b=14�������ΪVA�Ĵ�������ΪVB������������Һ��Ϻ���Һ�����ԣ����������ϵVA ??????????????VB����Ϻ���Һ�е�����Ũ�ȹ�ϵΪc��Na+��????????????c��CH3COO��)��???
��4����A�Ļ�ѧʽΪHR��B�Ļ�ѧʽΪMOH����a+b=14�����ߵ������Ϻ���Һ�Լ��ԡ�������Һ�бض���һ�������ܷ���ˮ�⣬��ˮ�ⷴӦ�����ӷ���ʽΪ??????????????????��
�ο��𰸣���7�֣���1��pH="?7??" ?��a+b="??13??
�����������
�����Ѷȣ�һ��
4������� ijѧ����0.100 mol��L-1��KOH����Һ�ζ�δ֪Ũ�ȵ�����,������ɷֽ�Ϊ���¼���:
A����ȡ20.00 mL����������Һע��ྻ����ƿ,������2~3�η�̪;
B���ñ���Һ��ϴ�ζ���2~3��;
C����ʢ�б���Һ�ļ�ʽ�ζ��̶ܹ���,���ڵζ��ܼ���ʹ֮������Һ;
D��ȡ��KOH��Һע���ʽ�ζ������̶ȡ�0������2~3 mL;
E.����Һ������0����0�����¿̶�,���¶���;
F.����ƿ���ڵζ��ܵ�����,�ñ�KOH��Һ�ζ����յ㲢���µζ���Һ��Ŀ̶ȡ�
�ʹ�ʵ��������:
(1)��ȷ���������˳����(����ĸ�����д)��������������������?
(2)����B���������Ŀ������������������������������������������?
(3)����A�������֮ǰ,�����ô�����Һ��ϴ��ƿ,��ζ��������������(�ƫ�ߡ���ƫ�͡����䡱)��?
(4)�жϵ���ζ��յ��ʵ����������������������������������������������?
�ο��𰸣�(1)B��D��C��E��A��F
(2)ϴȥ���ڵζ����ڱ�
���������(2)������ʢ�ű�Һ���Ǵ���Һ�ĵζ��ܾ�Ӧ��ϴ,��Ϊ�ζ��ܵ��ڱ��ϸ��ŵ�����ˮ�Ὣ�������Һϡ�Ͷ�����ⶨ��(3)A�������֮ǰ,���ô���Һϴ����ƿ,��ʹ����Һ���������20.00 mL,���ı�Һ��,��ⶨ���ƫ�ߡ�(4)�����÷�̪��ָʾ��,�ʵ���Һ����ɫ��Ϊdz��ɫ,�Ұ�����ڲ���ɫ,���ﵽ�˵ζ��յ㡣
�����Ѷȣ�һ��
5������� ��֪�����Ȼ�ѧ����ʽ����H2��g�� +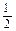 O2��g����H2O��l�� ��H="-285" kJ��mol-1
O2��g����H2O��l�� ��H="-285" kJ��mol-1
��H2��g�� +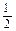 O2��g����H2O��g�� ��H="-241.8" kJ��mol-1 ��C��s�� +
O2��g����H2O��g�� ��H="-241.8" kJ��mol-1 ��C��s�� + O2��g����CO��g�� ��H="-110.5" kJ��mol-1
O2��g����CO��g�� ��H="-110.5" kJ��mol-1
�� C��s�� +O2��g����CO2��g�� ��H="-393.5" kJ��mol-1 �ش��������⣺
��1��H2��ȼ����Ϊ ��C��ȼ����Ϊ ��
��2��ȼ��1gH2����Һ̬ˮ���ų�������Ϊ ��
��3��д��COȼ�յ��Ȼ�ѧ����ʽ ��
�ο��𰸣���1��285 393��5
�����������
�����Ѷȣ�һ��