微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)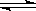 2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据右图可得出的判断结论正确的是???
2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据右图可得出的判断结论正确的是???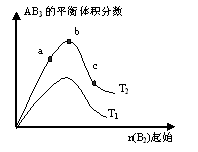 ????
????
A.正反应一定是放热反应
B.达到平衡时A2的转化率大小为:b>a>c
C.若T2>T1,则正反应一定是吸热反应
D.b点时,平衡体系中A、B原子数之比接近3∶1
参考答案:C
本题解析:
试题分析:A、由于不知道T2与T1的大小关系,所以不能判断反应时吸热还是放热,故错B、曲线先增加,原因是加入气体B2时,平衡正向移动。然后曲线再降低,原因是通入的气体量大,总气体体积增大显著。使得AB3的体积分数减小,实际上平衡仍旧在向正向移动,所以转化率比较应该是c>b>a。故错。
C、若T2>T1,温度越高,平衡时含量AB3越多,平衡正移,则正反应是吸热反应,故正确。
D、b点时,平衡体系中A、B原子数之比接近1∶3故错
点评:本题难度适中,利用勒夏特列原理来解题,注意温度对化学平衡的影响。本题需要把图像看懂,首先看横纵坐标,再看曲线的变化,再分析变化的原因。
本题难度:一般
2、选择题 .能影响水的电离平衡,并使溶液中c(H+)>c(OH-)的措施是????????????????????
A.将水加热煮沸,测得pH=6
B.向纯水中投入一小块金属钠
C.向水中加入NH4Cl固体
D.向水中加入Na2CO3固体
参考答案:C
本题解析:A?将水加热煮沸,虽然pH=6,但成中性,c(H+)=c(OH-)
B 2Na+2H2O=2NaOH+H2溶液成碱性 c(H+)<c(OH-)
C 向水中加入NH4Cl固体? NH4+水解显酸性c(H+)>c(OH-)
D 向水中加入Na2CO3固体,CO32-水解,溶液显碱性 c(H+)<c(OH-)
本题难度:简单
3、选择题 在KI溶液中存在下列平衡:I2(aq)+I-(aq)=I(aq)。测得不同温度下该反应的平衡常数K如表所示,下列说法正确的是
t/℃
| 5
| 15
| 25
| 35
| 50
|
K
| 1 100
| 841
| 689
| 533
| 409
?
A.反应I2(aq)+I-(aq) I(aq)的ΔH>0 I(aq)的ΔH>0
B.其他条件不变,升高温度,溶液中c(I)减小
C.该反应的平衡常数表达式为K=
D.25 ℃时,向溶液中加入少量KI固体,平衡常数K小于689
参考答案:B
本题解析:
由题意知,温度升高,平衡常数减少,则平衡向逆方向移动,正反应为放热反应,A错;其他条件不变,升高温度,平衡向逆方向移动,溶液中c(I3-)减少,B正确;该反应的平衡常数表达式为K= c(I3-)/[ c(I-)c(I2)],C错;平衡常数只与温度有关,加放少量的KI固体对平衡没有影响,D错;答案选B。
本题难度:一般
4、计算题 在密闭容器中将NO2加热到某温度时,进行如下的反应:2NO2 2NO+O2,反应5分钟后达平衡,测得平衡时各组分的浓度分别为:c(NO2)=0.06 mol/L,c(NO)=0.24 mol/L。 2NO+O2,反应5分钟后达平衡,测得平衡时各组分的浓度分别为:c(NO2)=0.06 mol/L,c(NO)=0.24 mol/L。
试求:
(1)NO2的转化率为?
(2)反应前后的压强比为多少?
(3)用O2来表示的反应速率是多少mol・L-1・min-1
参考答案:(1)80%
(2)P前/P后= 5/7
(
本题解析:
本题难度:一般
5、选择题 当把晶体N2O4放入密闭容器中气化,并建立了N2O4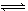 2NO2平衡后,保持温度不变,再通入若干N2O4气体,待反应达到新的平衡时,则新平衡与旧平衡相比,其 2NO2平衡后,保持温度不变,再通入若干N2O4气体,待反应达到新的平衡时,则新平衡与旧平衡相比,其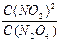 比值 比值
A.变大
B.不变
C.变小
D.无法确定
参考答案:B
本题解析:略
本题难度:简单
|