微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 500℃条件下,在恒容密闭容器中,充入1molNO2后达到如下平衡2NO2(g) N2O4(g)?,平衡后,向容器内再充入1mol N2O4(g),下列说法正确的(??????)
N2O4(g)?,平衡后,向容器内再充入1mol N2O4(g),下列说法正确的(??????)
A.容器内气体颜色先变浅后变深,最后比原来还要浅
B.反应向逆反应方向移动,所以NO2的百分含量增大
C.容器中的气体密度始终不变
D.N2O4的体积分数增大
参考答案:D
本题解析::
A 在恒容容器内气体颜色变化与有色气体的浓度有关,由c=n/v可知充入无色气体N2O4时由于NO2的浓度此刻没有变化,颜色不变,而后随着可逆反应的向正反应方向的进行,NO2浓度减小,再次达到平衡时气体颜色变浅。
B 在该反应条件下,充入N2O4相当于多体系增大压强,平衡向气体分子数减小的方向移动。
C 容器内气体的密度ρ="m/v" 充入N2O4增大了容器内气体的质量,使气体密度增大。
D 充入N2O4 ?平衡向正方向移动,使体系内N2O4的浓度增大,同样增大了其体积分数。
本题难度:一般
2、选择题 某一反应在一定条件下的平衡转化率为25.3%,其他条件不变,有一催化剂存在时,其转化率为
A.大于25.3%
B.小于25.3%
C.等于25.3%
D.约等于25.3%
参考答案:C
本题解析:考查外界条件对化学平衡状态的影响。催化剂能够同等程度改变正逆反应速率,所以使用催化剂不能改变平衡状态,即转化率是不变的,答案选C。
本题难度:困难
3、选择题 下列有关化学平衡图像描述正确的是????????????? ( )

A.图像A代表任何可逆反应中生成物浓度随温度的变化关系图
B.图像B表示反应的化学方程式为:2Z(s)  3X(g)+2Y(g)
3X(g)+2Y(g)
C.图像C代表在10 L容器、850℃时反应,到4 min时,反应放出51.6 kJ的热量
D.图像D代表等物质的量的气体A和B,在一定温度下发生反应A(g)+xB(g)  2C(g),达到平衡后,只改变反应的一个条件,其在20~40 min之间的平衡常数不相等
2C(g),达到平衡后,只改变反应的一个条件,其在20~40 min之间的平衡常数不相等
参考答案:C
本题解析:A项,只代表正反应是吸热反应的图像,故不正确;B项,反应物Z不一定是固体,且Z的化学计量数为3,不正确;C项,正确;D项,由图像知,A、B的化学计量数相等,则x=1,30 min时A、B、C的浓度均减小且减小幅度相同,故采用减小压强的措施,此时平衡常数不变,故不正确。
本题难度:一般
4、计算题 (10分).已知一氧化碳与水蒸气的反应为CO+H2O CO2+H2;在827℃时的平衡常数是100,如果反应开始时,一氧化碳和水蒸气的浓度都是0.011mol/L,计算:一氧化碳在此反应条件下的平衡转化率。
CO2+H2;在827℃时的平衡常数是100,如果反应开始时,一氧化碳和水蒸气的浓度都是0.011mol/L,计算:一氧化碳在此反应条件下的平衡转化率。
参考答案:9.09%
本题解析:
试题分析:???????? CO????+ ??H2O???=?? CO2???+?? H2
起始浓度(mol/l)?? 0.011????? 0.011???????? 0??????? 0
转化浓度(mol/l)??? x????????? x??????????? x??????? x
平衡浓度(mol/l)0.011-x ??0.011-x????????x???????x
因为
所以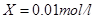
因此转化率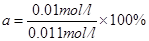 =9.09%
=9.09%
点评:在进行可逆反应的有关计算时,一般采用“三段式”进行,即分别列出起始量、转化量和平衡量或某深刻的量,然后依据已知条件列式计算即可。
本题难度:一般
5、选择题 t℃时,浓度都是 1mol / L 的气体X2 和Y2 ,在密闭容器中反应生成气体Z 。反应 2 min 后,测得参加反应的X2 为 0.6 mol / L ,用Y2 的变化表示的反应速率为 0.1 mol / (L・min) ,生成Z 的浓度为 0.4 mol / L ,则该反应的化学方程式是 [???? ]
A.3X2+Y2= 2X3Y
B.X2+2Y2= 2XY2
C.2X2+Y2= 2X2Y
D.X2 +3Y2= 2XY3
参考答案:A
本题解析:
本题难度:一般