微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 21.化学中通常用图像直观地描述化学反应进程或结果。下列图像及描述正确的是
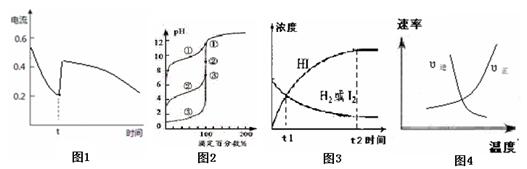
A.图1表示Zn-Cu原电池反应过程中的电流强度的变化,t时可能加入了双氧水
B.图2表示用0.1000mol・L-1NaOH溶液滴定浓度相同的三种一元酸,曲线①的酸性最强
C.图3表示可逆反应:H2(g)+I2(g)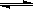 2HI(g)在一段时间内,各组分浓度的变化图,t1时刻速率关系为:υ正=υ逆
2HI(g)在一段时间内,各组分浓度的变化图,t1时刻速率关系为:υ正=υ逆
D.图4表示可逆反应:N2(g)+O2(g)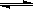 2NO(g)ΔH <0 ,正、逆反应速率随温度变化的曲线图
2NO(g)ΔH <0 ,正、逆反应速率随温度变化的曲线图
参考答案:A
本题解析:
试题分析:双氧水具有强氧化性,能加快反应速率;酸性越强,滴定曲线变化越明显,所以③的酸性是最强的;t1时刻只是浓度相等,并不是速率相等;升高温度,正、逆反应速率都增大。
考点:原电池、酸碱中和滴定曲线、速率曲线
点评:要学会根据图形图像来进行判断,本提要清楚原电池的工作原理,反应速率曲线的变化特点。
本题难度:一般
2、填空题 (1)室温下,在pH=12的NaCN溶液中,由水电离的c(OH-)为___________mol・L-1? 。
(2)等体积的下列溶液中,阳离子的总物质的量最大的是__________(填序号)。
①?0.2?mol・L-1的CuSO4溶液?????????
②?0.1?m?ol・L-1的Na2CO3
③?0.2?mol・L-1的KCl????????????????
④?0.1?mol・L-1的Na2SO4
(3)浓度为0.100?mol・L-1的下列各物质的溶液中,c(NH4+)由大到小的顺___________。(填序号)。
①NH4Cl?????②NH4HSO4?????③NH3・H2O????④CH3COONH4??
(4)?水的电离平衡如图所示:

①若A点表示25℃时水的电离平衡状态,当温度上升到100℃时,水的电离平衡状态到达B点。则此时水的离子积从_________增?加到__________。
②100℃时,若10体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前,该强酸的pH值pH1与强碱的pH值pH2之间应满足的关系是__________。
参考答案:(1)10-2??????????
(2)①????
本题解析:
本题难度:一般
3、填空题 (1) 在一定温度下,测得0.1 mol・L-1CH3COOH溶液的PH为3.0。则CH3COOH在水中的电离为 ,此温度CH3COOH的电离平衡常数为 。
(2) 在25℃时,Kw=1.0×10-14,测得0.1 mol・L-1 Na2A溶液的pH=7。则H2A在水溶液中的电离方程式为 ,该温度下,将0.01 mol・L-1 H2A溶液稀释到20倍后,溶液的pH= 。
(3) 已知HCN(aq)+NaOH(aq)=NaCN(aq)+ H2O(l) ΔH=-12.1 kJ・mol-1;
HCl(aq) +NaOH(aq)=NaCl(aq) + H2O(l) ΔH=-57.3 kJ・mol-1。
则在水溶液中HCN H++CN-电离的ΔH为 kJ・mol-1
H++CN-电离的ΔH为 kJ・mol-1
参考答案:(1) 1% 10-5 (2) H2A
本题解析:
试题分析:(1)CH3COOH CH3COO-+H+。PH=3.0,C(H+)=10-3mol/LC(CH3COOH)=0.1mol/L所以CH3COOH在水中的电离度为10-3mol/L÷0.1mol/L×100%=1%.在此温度下CH3COOH的电离平衡常数为(10-3mol/L)2/0.1mol/L=10-5mol/L.(2) 在25℃时,Kw=1.0×10-14,测得0.1 mol・L-1 Na2A溶液的pH=7,说明H2A是强酸。所以H2A在水溶液中的电离方程式H2A=2H++A2-。将0.01 mol・L-1 H2A溶液稀释到20倍后,则C(H+)=(2×0.01mol/L)÷20=0.001mol/L,所以溶液的pH=3。(3)若HCN为强酸,则它与NaOH反应产生1mol的水放出热量也是57.3 kJ・mol-1。现在放出热量12.1 kJ・mol-1,比强酸与氢氧化钠反应放出的热量少45.2KJ/mol.,说明在水溶液中HCN电离吸收热量为45.2KJ/mol.所以HCN
CH3COO-+H+。PH=3.0,C(H+)=10-3mol/LC(CH3COOH)=0.1mol/L所以CH3COOH在水中的电离度为10-3mol/L÷0.1mol/L×100%=1%.在此温度下CH3COOH的电离平衡常数为(10-3mol/L)2/0.1mol/L=10-5mol/L.(2) 在25℃时,Kw=1.0×10-14,测得0.1 mol・L-1 Na2A溶液的pH=7,说明H2A是强酸。所以H2A在水溶液中的电离方程式H2A=2H++A2-。将0.01 mol・L-1 H2A溶液稀释到20倍后,则C(H+)=(2×0.01mol/L)÷20=0.001mol/L,所以溶液的pH=3。(3)若HCN为强酸,则它与NaOH反应产生1mol的水放出热量也是57.3 kJ・mol-1。现在放出热量12.1 kJ・mol-1,比强酸与氢氧化钠反应放出的热量少45.2KJ/mol.,说明在水溶液中HCN电离吸收热量为45.2KJ/mol.所以HCN H++CN-电离的ΔH为+45.2kJ・mol-1。
H++CN-电离的ΔH为+45.2kJ・mol-1。
考点:考查弱电解质的电离度、电离平衡常数及溶液稀释问题的知识。
本题难度:一般
4、选择题 下列电离方程式正确的是( )
A.CaCl2=Ca2++Cl2?
B.Na2SO4=Na++SO42-
C.HNO3=H++NO3-
D.KOH=K++O2-+H+
参考答案:C
本题解析:
本题难度:简单
5、选择题 室温下,甲、乙两烧杯均盛有5mLpH=3的某一元酸溶液,向乙烧杯中加水稀释至pH=4。关于甲、乙两烧杯中溶液的描述正确的是
A.水电离出的OH-浓度:10c(OH-)甲 ≤ c(OH-)乙
B.溶液的体积:10V甲 ≤ V乙
C.若分别用等浓度的NaOH溶液完全中和,所得溶液的pH:甲 ≤ 乙
D.若分别与5mLpH=11的NaOH溶液反应,所得溶液的pH:甲 ≥ 乙
参考答案:B
本题解析:
试题分析:酸溶液中的氢氧根离子是水电离的,则pH=3的酸中,水电离的氢氧根离子浓度为,c(OH-)=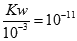 pH=4的酸中,水电离的氢氧根离子浓度为10-10mol/L,水电离出的OH-浓度:10c(OH-)甲 =c(OH-)乙,故A错误;B.若酸为强酸,则依据溶液吸稀释过程中氢离子浓度不变5ml×10-3=V×10-4,解得V=5Oml,则10V甲=V乙,若酸为弱酸,加水稀释时,促进弱酸的电离,电离产生的氢离子增多,要使pH仍然为4,加入的水应该多一些,所以10V甲<V乙,所以10V甲≤V乙,故B正确;C.稀释前后甲乙两个烧杯中所含的一元酸的物质的量相等,依据酸碱中和反应可知,消耗氢氧化钠的物质的量相等,生成的酸盐的浓度甲>乙,若酸为强酸,则二者的pH相等,若酸为弱酸,则甲溶液的pH大于乙,即:甲≥乙,故C错误;D.若酸是强酸,分别与5mL pH=11的NaOH溶液反应,恰好发生酸碱中和,生成强酸强碱盐,pH值相等,若为弱酸,则反应后酸有剩余,甲中剩余酸浓度大,酸性强,pH小,所得溶液的pH:甲≤乙,故D错误;故选B.
pH=4的酸中,水电离的氢氧根离子浓度为10-10mol/L,水电离出的OH-浓度:10c(OH-)甲 =c(OH-)乙,故A错误;B.若酸为强酸,则依据溶液吸稀释过程中氢离子浓度不变5ml×10-3=V×10-4,解得V=5Oml,则10V甲=V乙,若酸为弱酸,加水稀释时,促进弱酸的电离,电离产生的氢离子增多,要使pH仍然为4,加入的水应该多一些,所以10V甲<V乙,所以10V甲≤V乙,故B正确;C.稀释前后甲乙两个烧杯中所含的一元酸的物质的量相等,依据酸碱中和反应可知,消耗氢氧化钠的物质的量相等,生成的酸盐的浓度甲>乙,若酸为强酸,则二者的pH相等,若酸为弱酸,则甲溶液的pH大于乙,即:甲≥乙,故C错误;D.若酸是强酸,分别与5mL pH=11的NaOH溶液反应,恰好发生酸碱中和,生成强酸强碱盐,pH值相等,若为弱酸,则反应后酸有剩余,甲中剩余酸浓度大,酸性强,pH小,所得溶液的pH:甲≤乙,故D错误;故选B.
考点:电离平衡与PH计算
本题难度:一般