微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 向2.0L恒容密闭容器中充人1.0mol PCl5,在温度为T时发生如下反应
PCl5(g)  PCl3(g)+C12(g)?
PCl3(g)+C12(g)?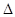 H=124kJ・mol-1。反应过程中测定的部分数据见下表:
H=124kJ・mol-1。反应过程中测定的部分数据见下表:
时间t/s
| 0
| 50
| 150
| 250
| 350
|
n(PCL3)/mol
| 0
| 0.16
| 0.19
| 0.2
| 0.2
?
回答下列问题
(1)反应在前50 s的平均速率v(PCI5)=________。
(2)温度为T时,该反应的化学平衡常数=________。
(3)要提高上述反应的转化率,可采取的措施有________。
(4)在温度为T时,若起始时向容器中充入0.5mol PCl5和a mol Cl2平衡时PCl5的转化率仍为20%,则a=________。
(5)在热水中,五氯化磷完全水解,生成磷酸(H3 PO4),该反应的化学方程式是________。
若将0.01 mol PCI5投入l L热水中,再逐滴加入AgNO3溶液,先产生的沉淀是________ [已知Ksp(Ag3 PO4)="1.4" x 1 0-16,Ksp(AgCl)="1.8" x 10-10]。
(6)一定条件下,白磷溶于硝酸溶液产生一种氮氧化合物气体,该气体与白磷的物质的量之比为20:3,反应的化学方程式为____________________________。
参考答案:
(1)0.0016 mol/( L・s) (2)0.
本题解析:
试题分析:(1)反应在前50 s的平均速率v(PCI3)=Δc/Δt=0.16mol÷2.0L÷50s=0.0016mol/(L・s).由于v(PCI5)= v(PCI3)= 0.0016 mol/( L・s).由表中数据可以看出,在温度为T,当反应达到平衡时,n(PCI3)=" 0.2mol" ,n(C12)=0.2mol.,n(PCI5)=0.8mol.所以c(PCI5)=0.4mol/L;c(PCI3)=0.1mol/L;c(C12)=0.1mol/L,所以化学平衡常数 本题难度:一般 本题难度:一般
2、选择题 某一化学反应在体积为2L的恒容密闭容器中进行,反应物气体B的物质的量在5 s内从8.0 mol变成2.0 mol,在这5 s内B的化学反应速率为(??)
A.3 mol?L-1?s-1
B.0.3 mol?L-1?s-1
C.0.6 mol?L-1?s-1
D.0.1 mol?L-1?s-1
参考答案:C
本题解析:反应速率通过用单位时间内浓度的变化量来表示,所以B的反应速率为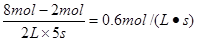 ,即选项C是正确的,答案选C。 ,即选项C是正确的,答案选C。
本题难度:一般
3、选择题 实验室用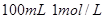 盐酸与锌粉反应,下列措施能使反应速率加快的是 盐酸与锌粉反应,下列措施能使反应速率加快的是
A.降低温度
B.改用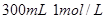 盐酸 盐酸
C.改用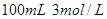 盐酸 盐酸
D.用等量锌粒代替锌粉
参考答案:C
本题解析:考查外界条件对反应速率的影响。在其他条件不变的时,增大反应物的浓度或升高温度或增大反应物的接触面积等均可以加快反应速率,所以选项C正确。
本题难度:一般
4、选择题 决定化学反应速率的主要因素是
[???? ]
A.反应温度
B.使用催化剂
C.外界压强
D.反应物的性质
参考答案:D
本题解析:
本题难度:简单
5、选择题 在密闭容器中进行合成氨的反应,达到平衡后,将体系中各物质的浓度增大到原来的2倍,则产生的结果是
A.平衡向正反应方向移动
B.平衡向逆反应方向移动
C.平衡不移动
D.NH3的百分含量增加
参考答案:AD
本题解析:试题分析:达到平衡后,将体系中各物质的浓度增大到原来的2倍,相当于是将容器的容积缩小到原来的2倍,即相当于是加压,因此平衡向正反应方向移动,生成物的百分含量增加,答案选AD。
考点:考查外界条件对平衡状态的影响
点评:本题是基础性试题的考查,难度不大。主要是训练灵活运用知识的能力,有利于调动学生的学习积极性和学习兴趣。
本题难度:一般
|