��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���淴Ӧ2SO2+O2?

?2SO3���ܱ������дﵽ��ƽ�⣬����˵����ȷ���ǣ�������
A��SO2��O2���ٻ��ϣ���Ӧֹͣ��
B��������ѹǿ���ֲ���
C��SO2��O2��SO3��Ũ�����
D��SO2��O2��SO3�����ʵ���֮��Ϊ2��1��2
�ο��𰸣�A����ѧƽ���Ƕ�̬ƽ�⣬����Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������
���������
�����Ѷȣ���
2��ѡ���� ��һ�������£���Ӧ?2SO2��g��+O2��g��

2SO3��g���ﵽ�����ʱ������˵����ȷ���ǣ�������
A����Ӧ��ȫֹͣ�����ټ�������
B���������SO2��O2��SO3�ķ�������Ϊ2��1��2
C�����µ�ѹ�£���������Ϊ��ʼʱ������֮��
D����Ӧ������ƽ��Ħ���������ٸı�
�ο��𰸣�A����ѧ��Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ�����Ӧû��ֹͣ
���������
�����Ѷȣ���
3������� ��1������ý(V2O5)�ܼӿ�SO2���������ʣ��˹�����SO2����V2O5��Ӧ����V2O4���ù��̵Ļ�ѧ����ʽ�ɱ�ʾΪ__________________________________________��
��2��Ϊ�ⶨ�����л������SO2���������ѡ��0.0500 mol/L I2�ı���Һ��������Һ���вⶨ����֪��V������I2����Һ��="10.00" mL��V���ɼ�������="100.0" mL��������Ϊ��״��������������SO2?���������Ϊ_____________________��
��3��һ���¶�ʱ��SO2��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ��ͼ9��ʾ���Է�����ҵ�����в��ó�ѹ��ԭ����____________________��
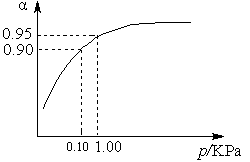
ͼ9
��4�����¶���ͬ�������Ϊ1 L�������ܱ������У�����ͬ��ʽͶ�뷴Ӧ����ֺ��¡����ݣ���÷�Ӧ�ﵽƽ��ʱ���й��������¡�
��֪��2SO2(g)+O2(g) 2SO3(g)??��H ="-98.3" kJ��mol-1��
2SO3(g)??��H ="-98.3" kJ��mol-1��
��?��
| ��
| ��
| ��
|
��Ӧ��Ͷ����
| 2 mol SO2��1 mol O2
| 2 mol SO3
| m mol SO2��n mol O2��
p mol SO3
|
c(SO3) /mol��L-1
| 1.4
| 1.4
| 1.4
|
�����仯
| �ų�a kJ
| ����b kJ
| ����c kJ
|
SO2��SO3��ת����
| ��1
| ��2
| 12.5%
?
����1+��2=_________________��p=________________mol��b+c=_______________kJ��
�ο��𰸣���1��SO2+V2O5 �����������1�����ݷ�Ӧ����������֪������ʽΪSO2+V2O5 �����������1�����ݷ�Ӧ����������֪������ʽΪSO2+V2O5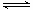 SO3+ V2O4�� SO3+ V2O4��
��2��SO2�͵ⷴӦ�ķ���ʽΪSO2��I2��2H2O=H2SO4��2HI,����SO2�����ʵ�����0.0500 mol/L��0.01L��0.0005mol���������0.0005mol��22.4L/mol��0.0112L������������S
�����Ѷȣ�һ��
4��ѡ���� ��һ���¶��£����淴ӦA��g��+3B��g��?2C��g���ﵽƽ��״̬�ı�־�ǣ�������
A��C���ɵ�������A�ֽ���������
B����λʱ������nmolA��ͬʱ����3nmolB
C��A��B��C��Ũ�Ȳ��ٱ仯
D��A��B��C�ķ�������Ϊ1��3��2
�ο��𰸣�A���Կ��淴ӦX��g��+3Y��g���T2Z��g����˵��C���ɵ�
���������
�����Ѷȣ�һ��
5������� ����β���ﺬ�е�NO������������ȼ��ȼ�յĸ�����������������Ӧ���£� N2(g)��O2(g)?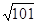 2NO(g)����H>0����֪�÷�Ӧ��2 404 �� ʱ��ƽ�ⳣ��K��64��10��4����ش� 2NO(g)����H>0����֪�÷�Ӧ��2 404 �� ʱ��ƽ�ⳣ��K��64��10��4����ش�
��1��ij�¶��£���2L���ܱ������г���N2��O2��1mol��5���Ӻ�O2�����ʵ���Ϊ0.5mol����N2�ķ�Ӧ����________��
��2���ٶ��÷�Ӧ���ں��������½��У��жϸ÷�Ӧ�ﵽƽ��ı�־________��
A������1 mol N2ͬʱ����1 mol O2
B����������ܶȲ���
C���������ƽ����Է�����������
D��2v(N2)����v(NO)��
��3����N2��O2�Ļ�����������º����ܱ������У����б仯������ȷ����________(����ĸ���)��
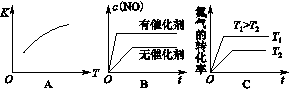
��4������º��ݵ��ܱ������г�������ʵ�����N2��O2���ﵽƽ��״̬���������г���һ����NO�����´ﵽ��ѧƽ��״̬����ԭƽ��״̬��ȣ���ʱƽ��������NO���������______��(������С�����䡱)
��5�����¶��£�ijʱ�̲��������N2��O2��NO��Ũ�ȷֱ�Ϊ2.5��10��1mol/L��4.0��10��2mol/L��3.0��10��3mol/L����ʱ��Ӧ___________(����ڻ�ѧƽ��״̬������������Ӧ������С������淴Ӧ������С�)��������____
�ο��𰸣���1��0.05 mol/(L��min)����2��A��D����3��
���������
�����������1�� V(N2)=��C(N2)�¦�t="(0.5mol��2L)��5min=0.05" mol/(L��min)����2��A�����ݷ�Ӧ����ʽ��֪������1 mol N2ͬʱ������1 mol O2��������1 mol O2�����������������������������ȣ���Ӧ�ﵽƽ��״̬����ȷ��B����Ϊ��Ӧ���ں��������½��У���Ӧǰ�����������Ҳ���䣬�������۷�Ӧ�Ƿ�ﵽƽ�⣬��������ܶȲ��䣬��˲�����Ϊ�ж�ƽ��ı�־������C����Ϊ��������ʵ������䣬����Ҳ���䣬���Ի������ƽ����Է����������䲻����Ϊ�ж�ƽ
�����Ѷȣ�һ��
|