��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��֪
��1����H2(g)+ O2(g)=H2O(g) ��H1="a" KJ/mol
��2��2H2(g)+ O2(g)=2H2O(g) ��H2="b" KJ/mol
��3��H2(g)+ O2(g)=H2O(l) ��H3="c" KJ/mol
��4��2H2(g)+ O2(g)=2H2O(l) ��H4="d" KJ/mol
���й�ϵʽ��ȷ���ǣ� ��
A��a��c��0
B��b��d��0
C��2a="b��0"
D��2c=d��0
2��ѡ���� ��֪���Ȼ�ѧ����ʽ��SO2��g��+
1
2
O2��g���TSO3��g����H=-98.32kJ/mol����4molSO2�μӷ�Ӧ�����ų�314.3kJ����ʱ��SO2��ת������ӽ��ڣ�������
A��40%
B��50%
C��80%
D��90%
3��ѡ���� ���ܻ�ѧ��Ӧ������һ����ɻ��Ƿ�Ϊ������ɣ�������̵���ЧӦ����ͬ�ġ�
��֪��H2O(g)===H2O(l)����H1����Q1 kJ��mol��1��
C2H5OH(g)===C2H5OH(l)����H2����Q2 kJ��mol��1��
C2H5OH(g)��3O2(g)===2CO2(g)��3H2O(g)����H����Q3 kJ��mol��1��
��ʹ23 g�ƾ�Һ����ȫȼ�գ����ָ������£���ų�������Ϊ(����)
A��(Q1��Q2��Q3) kJ
B��[0.5(Q1��Q2��Q3)] kJ
C��(0.5Q1��1.5Q2��0.5Q3) kJ
D��(1.5Q1��0.5Q2��0.5Q3) kJ
4������� SO2��NOx�ڻ�ѧ��ҵ������Ҫ��;��Ҳ�Ǵ�����Ⱦ����Ҫ��Դ�����������ò��أ�Ԥ�������������ǵ�ǰ��ҵ�Ϻͻ������������о�����Ҫ����֮һ��
��1���ڽӴ���������Ĺ����У�����2SO2(g)��O2(g)  2SO3(g) ��H��0��Ӧ��ij�¶��£�SO2��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ����ͼ��ʾ������ͼʾ�ش��������⣺ 2SO3(g) ��H��0��Ӧ��ij�¶��£�SO2��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ����ͼ��ʾ������ͼʾ�ش��������⣺
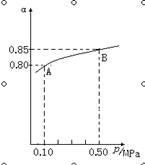
��ƽ��״̬��A��Bʱ��ƽ�ⳣ��K(A) K(B)�����������������������
�ڽ�2��0molSO2��1��0molO2����10L���ܱ������У���40s��Ӧ�ﵽƽ�⣬��ʱ��ϵ��ѹǿΪ0��10MPa����һ��ʱ����SO2��ƽ����Ӧ����Ϊ ��
�÷�Ӧ��ƽ�ⳣ��Ϊ ��
��2����CH4����ԭNOx�������������������Ⱦ�����磺CH4(g)��4NO2(g) �� 4NO(g)��CO2(g)��2H2O(g) ��H��-574kJ��mol��1
CH4(g)��4NO(g) �� 2N2(g)��CO2(g)��2H2O(g) ��H��-1160kJ��mol��1
ȡ��״����4��48LCH4��ʹ֮��ȫ��Ӧ��
������NO2��ԭ��N2������������ת�Ƶ��ӵ����ʵ���Ϊ ��
������ԭNO2��NO�Ļ����ų���������Q��ȡֵ��Χ�� ��
5��ѡ���� ���л�ѧ������ȷ����
[???? ]
A����ʾ��Ȳ��ȼ���ȡ���Ӧ���Ȼ�ѧ����ʽ��C2H2 (g)+ O2(g)=2CO2(g)+H2O(g) ��H =-1 256kJ/mol
B��Na2O2�ĵ���ʽ��
C���������������Һ�����缫�������ĵ缫��ӦʽΪ��Fe-3e-+3OH-=Fe(OH)3
D����ʾ�к��ȵ��Ȼ�ѧ����ʽ��NaOH( aq)+ H2SO4(aq)=Na2SO4(aq)+H2O(l) ��H=- 57. 3kJ/mol
|