��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������巴ӦmA��g����nB��g��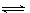 pC��g����qD��g����H?������4��ͼ���У�ͼ��Ӧ�������ȷ���ǣ�???��
pC��g����qD��g����H?������4��ͼ���У�ͼ��Ӧ�������ȷ���ǣ�???��

A��ͼ�ٱ�ʾ��Ӧ������Ӧ��ʼ��m��n��p��q
B��ͼ�ڱ�ʾ��Ӧ���淴Ӧ��ʼ����H��0
C��ͼ�۱�ʾ��Ӧ���淴Ӧ��ʼ����H��0
D��ͼ�ܱ�ʾ��Ӧ������Ӧ��ʼ�����������뷴Ӧ�ıȽ�
�ο��𰸣�B
���������A��B%���㿪ʼ����˵����Ӧ�Ǵ��淴Ӧ��ʼ������ȷ
B��B%���㿪ʼ����˵����Ӧ�Ǵ��淴Ӧ��ʼ��T1�¶����ȴﵽƽ�⣬˵��T1����T2������ʱB%��С����ƽ�������ƶ�������ӦΪ���ȷ�Ӧ����H��0����ȷ
C��C%�ɴ��С��˵��ƽ�������ƶ�����������˵����Ӧ�Ǵ���һ����ʼ���ų�
D������ֻ�ܸı����ʣ������ܸı�ƽ�⼰�����ʵĺ���������ȷ
��ΪB
�����Ѷȣ�һ��
2�������� ��һ���¶��½�100���̣Σ����ȣ�����������ܱպ�ѹ�����ڣ�������Ӧ�ﵽƽ��ʱά���¶Ȳ��䣬��û�������ܶ��Ƿ�Ӧǰ�ܶȵ�1��25����ƽ��������Ϊ15��5����ƽ��ʱ�Σ���ת���ʣ��Σ����ȣ��������忪ʼʱ��Ϊ���ٺ���?
�ο��𰸣�ƽ��ʱ�Σ���ת����25�����Σ����ȣ��������忪ʼ������ֱ�Ϊ
�����������ͬ��ͬP���У��ѣ����ѣ�������������������

�������� ��1��1��25������������15��5��?������12��4
���֣����֣�������n����n����
��������?�֣Σ��ã֣ȣ���10��4��15��6
������?�֣Σ���10��4����10��4��15��6����100mL��40����
����??�֣ȣ���100mL��40mL��60����
������Σ�ת�������Ϊ�������У�
����?????�Σ�?������?3�ȣ�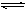 2�Σȣ�
2�Σȣ�
������ʼ�����40������������60��������0
����ת���������������������3��������2��
����ƽ�������40����������60��3������2��
����?���ܣ�40������60��3����2����100��2��
��������
����15��5������40��������28����60��3������2��2����17������100��2����
�������?����10����
������Σ���ת����Ϊ��
������������10��40����100����25��
�����Ѷȣ���
3��ѡ���� ���ڴﵽƽ��״̬�Ŀ��淴Ӧ��N2+3H2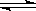 2NH3(����ӦΪ���ȷ�Ӧ)����������ȷ����
2NH3(����ӦΪ���ȷ�Ӧ)����������ȷ����
A����Ӧ����������Ũ�����
B��N2��H2��Ũ��֮��һ��Ϊ1��3
C�������¶ȣ�ƽ��������NH3��Ũ������
D������ѹǿ�������ڰ��ĺϳ�
�ο��𰸣�C
�����������
�����Ѷȣ�һ��
4��ѡ���� CO2��H2�Ļ��������ȵ�850 ��ʱ���ɽ�������ƽ�⣺CO2 + H2 CO + H2O ��һ���¶��£�ƽ����90%��H2�����H2O����c(CO2)c(H2)=c(CO)c(H2O)����ԭ�������CO2��H2�ķ�����֮����
CO + H2O ��һ���¶��£�ƽ����90%��H2�����H2O����c(CO2)c(H2)=c(CO)c(H2O)����ԭ�������CO2��H2�ķ�����֮����
A��1��1
B��1��5
C��9��1
D��1��10
�ο��𰸣�C
�����������
�����Ѷȣ���
5��ѡ���� ��һ���¶��£����淴Ӧ2SO2+O2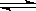 2SO3�ﵽƽ��״̬�ı�־��
2SO3�ﵽƽ��״̬�ı�־��
A��������SO2��O2��SO3�ķ�����֮��Ϊ2�s1�s2
B����λʱ��������nmol SO3��ͬʱ����n/2mol O2
C�������ڵ�ѹǿ����ʱ����仯
D������SO3������O2��������ͬ
�ο��𰸣�C
�����������
�����Ѷȣ�һ��