微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 [三选一选修3:物质结构与性质]????
血红素中含有C、H、O、N、Fe五种元素。回答下列问题: ???
(1)C、N、O、H四种元素中电负性最大的是__________(填元素符号),Fe2+稳定性比Fe3+稳定性__________(填“强”或“弱”),原因是________?。 ???
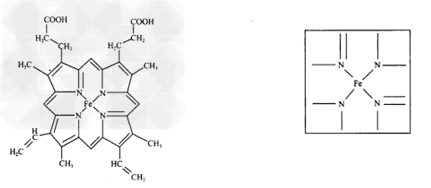
(2)下图所示为血红蛋白和肌红蛋白的活性部分――血红素的结构。血红素中N原子的杂化方式有_________,在下图的方框内用“→”标出Fe2+的配位键。??????
(3)NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69?pm和78?pm,则熔点NiO____FeO(填“<”“>”); ???
(4)根据等电子原理,写出N2O的电子式_________,分子的空间构型为__________。
(5)铁有δ、γ、α三种同素异形体,γ晶体晶胞中所含有的铁原子数为__________,δ、α两种晶胞中铁原子的配位数之比为____。
2、填空题 Mn、Fe均为第四周期过渡元素,两元素的部分电离能(I)数据列于下表:
| 元素 | Mn | Fe
|
电离能/kJ?mol-1
I1
717
759
I2
1509
1561
I3
3248
2957
回答下列问题:
(1)Mn元素价电子层的电子排布式为______,比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难.对此,你的解释是______.
(2)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物,则与Fe原子或离子形成配合物的分子或离子应具备的条件是______.
(3)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂,据此判断三氯化铁晶体为______晶体.
(4)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示.面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为______,其中体心立方晶胞空间利用率为______.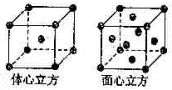
3、选择题 下列有关数据的比较,不正确的是( )
A.元素的价电子数总等于所在族的族序数
B.NaOH晶体中阳离子和阴离子数目相等
C.CsCl晶体中每个Cs+周围紧邻的Cl-和每个Cl-周围紧邻的Cs+个数相等
D.[Co(NH3)6]3+中的N原子数与配位键数相等
4、填空题 配位化学创始人维尔纳发现,将分别为1 mol的 CoCl3・6NH3(黄色)、CoCl3・5NH3(紫红色)、
CoCl3・4NH3(绿色)、CoCl3・4NH3(紫色)四种配合物溶于水,加入足量硝酸银溶液,立即有沉淀生成,生成的氯化银分别为3 mol、2 mol、1 mol 和l mol。已知上述配合物中配离子的配位数均为6。
(1)请根据实验事实用配合物的形式写出它们的化学式。
CoCl3・6NH3__________,CoCl3・5NH3____________,CoCl3・4NH3(绿色和紫色)____________。
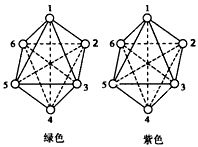
(2)后两种物质组成相同而颜色不同的原因是它们互为同分异构体,已知绿色的配合物内界结构对称,请在下图中用元素符号标出氯原子的位置。
5、选择题 配合物在许多方面有着广泛的应用。下列叙述不正确的是 [???? ]
A.以Mg2+为中心的大环配合物叶绿素能催化光合作用
B.Fe2+的卟啉配合物是输送O2的血红素
C.[Ag(NH3)2]+是化学镀银的有效成分
D.向溶液中逐滴加入氨水,可除去硫酸锌溶液中的Cu2+
|