��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��300��ʱ���ı���ʼ��Ӧ����n(H2)�Է�ӦN2(g) + 3H2(g)  2NH3(g)+Q��Q>0����Ӱ������ͼ��ʾ������˵����ȷ����
2NH3(g)+Q��Q>0����Ӱ������ͼ��ʾ������˵����ȷ����
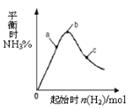
A����Ӧ��b��ﵽƽ��
B��b��H2��ת�������
C��c��N2��ת�������
D��a��b��c�����ƽ�ⳣ��Kb > Ka > Kc
2��ѡ���� һ���¶��£���2L�����ܱ������з�����Ӧ��2N2O5(g)  4NO2(g)+ O2(g)����H��0.��Ӧ��Ͳ�������������ʵ����淴Ӧʱ��仯��������ͼ��ʾ������˵����ȷ����
4NO2(g)+ O2(g)����H��0.��Ӧ��Ͳ�������������ʵ����淴Ӧʱ��仯��������ͼ��ʾ������˵����ȷ����

A��10minʱ����Ӧ�ﵽƽ��
B�����¶��·�Ӧ��ƽ�ⳣ��Ϊ8
C��0~20min��ƽ����Ӧ����v(N2O5)=0.05mol?L-1?min-1
D������a��ʾNO2�����ʵ����淴Ӧʱ��ı仯
3��ѡ���� �ϳɰ���ҵ�Թ��ú���ᷢչ������Ҫ�����塣�����ܱ������еķ�Ӧ��N2(g)+3H2(g) 2NH3(g)??��H<0��673K��30MPa��n(NH3)��n(H2)��ʱ��仯�Ĺ�ϵ����ͼ��ʾ������������ȷ����
2NH3(g)??��H<0��673K��30MPa��n(NH3)��n(H2)��ʱ��仯�Ĺ�ϵ����ͼ��ʾ������������ȷ����
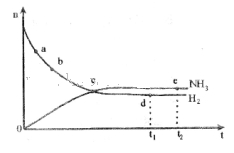
A����a������Ӧ���ʱȵ�b��С
B����c����Ӧ�ﵽƽ��
C����d��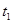 ʱ�̣��͵�e��
ʱ�̣��͵�e�� ʱ�̣���n(
ʱ�̣���n(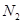 )��һ��
)��һ��
D�������������䣬773K�·�Ӧ��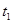 ʱ�̣�n(H2)����ͼ
ʱ�̣�n(H2)����ͼ
��d���ֵ��
4��ѡ���� ij�ܱ������г�������ʵ���������A��B��һ���¶��·�����ӦA(g)+xB(g)??????2C��g�����ﵽƽ���ֻ�ı䷴Ӧ��һ��������������������ʵ�Ũ�ȡ���Ӧ������ʱ��仯�Ĺ�ϵ����ͼ��ʾ������˵���в���ȷ����

A����30minʱ�����¶ȣ�40minʱ�����¶�
B��8minǰA��ƽ����Ӧ����Ϊ0.08 mol��L-1��min-1
C����Ӧ����ʽ�е�x=1������ӦΪ���ȷ�Ӧ
D��20min~40min��÷�Ӧ��ƽ�ⳣ����Ϊ4
5�������� ��2L���ܱ������з���4molN2O5���������·�Ӧ��2N2O5(g)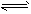 4NO2(g)+O2(g)����Ӧ5min���
4NO2(g)+O2(g)����Ӧ5min���
N2O5ת����20%����
��1���ԣ�NO2)����(O2���ֱ�Ϊ���٣�
��2��5minʱ��N2O5ռ�������������İٷֱ��Ƕ��٣�