微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用NA表示阿伏德罗常数,下列叙述正确的是
A.标准状况下,22.4L H2O含有的分子数为 NA
B.常温常压下,1.06g Na2CO3溶于水形成的溶液中含有Na+离子数为0.02 NA
C.通常状况下,NA个CO2分子占有的体积为22.4L
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为NA
参考答案:B
本题解析:考查阿伏德罗常数的应用。标准状况下,水不是气体,不能适用于气体摩尔体积,选项A不正确;1.06g碳酸钠的物质的量是1.06g÷106g/mol=0.01mol,则根据化学式可知,含有0.02mol钠离子,即钠离子个数是0.02 NA,选项B正确;选项C不正确,因为不是在标准状况下;选项D不正确,因为容易的体积不能确定,答案选B。
本题难度:一般
2、填空题 将红磷与氯气按1∶1.8的物质的量比混合,点燃使其充分燃烧,发生如下反应:2P+3Cl2 2PCl3、PCl3+Cl2
2PCl3、PCl3+Cl2 PCl5,完全反应后氯气没有剩余,则生成物中三氯化磷与五氯化磷的物质的量之比为??????。
PCl5,完全反应后氯气没有剩余,则生成物中三氯化磷与五氯化磷的物质的量之比为??????。
参考答案:7∶3
本题解析:根据化学反应方程式可得下列关系:
P???? ~??? PCl3???? ~???? 3Cl
x?????????? x?????????????3x
P???? ~??? PCl5???????~???? 5Cl
y?????????? y?????????????5y
根据题意可得: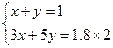
本题难度:简单
3、选择题 100mL 0.30mol/LNa2SO4溶液和50mL 0.20mol/LAl2(SO4)3溶液混合后,在相同温度下溶液中SO42-物质的量浓度为? [???? ]
A.0.20mol/L?????
B.0.25mol/L????
C.0.40mol/L????
D.0.50mol/L
参考答案:C
本题解析:
本题难度:简单
4、实验题 实验室配制500ml?? 2mol・L-1的H2SO4溶液
(1)500ml 2mol・L-1的H2SO4溶液中所含溶质的质量是???????g。
(2)配制时,所需仪器应该有烧杯、玻璃棒、量筒、????????????、???????????????。
(3)容量瓶在使用前,首先应检查???????????????????????。
(4)此实验中,玻璃棒的两个作用分别是?????????????、???????????????。
(5)下列操作会使配制的溶液浓度偏低的是??????????????(选填序号)
A.没有将洗涤液转移到容量瓶
B.定容时俯视刻度线
C.容量瓶洗净后未干燥
D.转移过程中有少量溶液测出
参考答案:(1)98。(2)500ml容量瓶(未写量程不得分)、胶头滴
本题解析:
试题分析:(1)500ml 2mol・L-1的H2SO4溶液中所含溶质的质量是0.5L×2mol/L×98g/mol=98g。
(2)配制时,所需仪器应该有烧杯、玻璃棒、量筒外,还需要500ml容量瓶和定容时的胶头滴管。
(3)容量瓶在使用前,首先应检查是否漏水(或漏液)。
(4)此实验中,玻璃棒的两个作用分别是,浓硫酸稀释时起搅拌作用。转移至容量瓶时,起引流作用。
(5)根据c=n/V可知,若没有将洗涤液转移到容量瓶中,则溶质减少,浓度偏低;定容时俯视刻度线,则容量瓶中溶
本题难度:一般
5、计算题 53克Na2CO3的物质的量是多少?所含Na+和CO32-的物质的量各是多少?
参考答案:0.5mol;1mol;o.5mol
本题解析:
本题难度:一般