微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在合成氨时,可以提高H2转化率的措施:
A.延长反应时间
B.充入过量H2
C.充入过量N2
D.升高温度
参考答案:C
本题解析:试题分析:延长反应时间,H2转化率不变,充入过量H2,H2转化率降低,充入过量N2,H2转化率升高,合成氨是放热反应,升高温度平衡逆向移动,H2转化率降低,所以答案选C。
考点:影响化学平衡移动的条件
点评:改变影响平衡移动的一个因素,平衡总是向减弱这种改变的方向移动。
本题难度:一般
2、选择题 有机物CH3―CH==CH―Cl能发生? ( )
①取代反应,②加成反应,③消去反应,④使溴水褪色,⑤使酸性KMnO4溶液褪色,⑥与AgNO3溶液生成白色沉淀,⑦聚合反应
A.以上反应均可发生
B.只有⑦不能发生
C.只有⑥不能发生
D.只有②不能发生
参考答案:C
本题解析:试题分析:此有机物含有碳碳双键,可使溴水、酸性KMnO4溶液褪色,可发生加成反应、聚合反应;含有官能团―Cl,可发生取代反应、消去反应。由于此有机物中氯原子不能电离出来,故不能与AgNO3溶液生成白色沉淀。所以选C。
考点:官能团的性质。
点评:熟悉各类官能团的性质。
本题难度:简单
3、选择题 在下列变化中,需要加入合适的氧化剂才能实现的是( )
A.HCl→H2
B.CO2→CO
C.Fe2O3→Fe
D.Br-→Br2
参考答案:D
本题解析:试题分析:根据选项中存在元素的化合价升高的变化可知,选项中的物质具有还原性,则需要加入合适的氧化剂来实现氧化还原反应。
A、HCl→H2中H元素的化合价降低,需要加入合适的还原剂来实现,如加入Zn,故A不选;
B、CO2→CO中C元素的化合价降低,需要加入合适的还原剂来实现,如加入碳,故B不选;
C、FeCl3→FeCl2中Fe元素的化合价降低,需要加入合适的还原剂来实现,如加入铁,故C不选;
D、SO2→SO3中S元素的化合价升高,则需要加入合适的氧化剂来实现,如加入氧气,故D选;
故选D。
考点:氧化还原反应
点评:本题考查氧化还原反应,明确还原剂、氧化剂中元素的化合价变化是解答本题的关键,并熟悉常见的氧化还原反应来解答.
本题难度:简单
4、计算题 (6分)Ⅰ.取1.43g Na2CO3・XH2O 溶于水配成10ml 溶液,然后逐滴滴入稀盐酸直至没有气体放出为止,用去盐酸 2.0ml,并收集到112ml CO2(标况)。
(1)稀盐酸物质的量浓度为___________。
(2)Na2CO3・xH2O的摩尔质量为___________。
(3)x=_______。
Ⅱ.在智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘,化学方程式是:
2NaIO3+5NaHSO3=3NaHSO4+2Na2SO4+I2+H2O
(1)用“双线桥”标出电子转移的方向和数目。
(2)反应产物中,氧化产物与还原产物的物质的量之比为 。
参考答案:Ⅰ. (1)5 mol・L-1(2)286g・mol-1(3
本题解析:
试题分析:Ⅰ.(1)n(CO2)=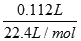 =0.005mol,
=0.005mol,
Na2CO3 + 2HCl = 2NaCl+CO2↑+H2O
1 2 1
n(Na2CO3) n(HCl) 0.005mol
(1)n(HCl)=2×n(CO2)=2×0.005mol=0.01mol,c(HCl)= =5.0mol/L,故答案为:5.0mol/L;(2)n(Na2CO3?xH2O)=n(Na2CO3)=0.005mol,M(Na2CO3?xH2O)=286g/mol,故答案为:286g/mol; (3)由摩尔质量可知:106+18x=286,x=10,故答案为:10.
=5.0mol/L,故答案为:5.0mol/L;(2)n(Na2CO3?xH2O)=n(Na2CO3)=0.005mol,M(Na2CO3?xH2O)=286g/mol,故答案为:286g/mol; (3)由摩尔质量可知:106+18x=286,x=10,故答案为:10.
Ⅱ.(1)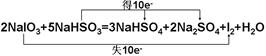
(2)反应中S元素的化合价升高,则S元素失去电子被氧化,生成硫酸钠,I元素的化合价降低,则NaIO3为氧化剂,由化合价变化可知生成1mol氧化产物转移2mol电子,生成1mol还原产物,转移10mol电子,根据转移电子数守恒知,氧化产物与还原产物的物质的量比为5:1.
考点:氧化还原反应
本题难度:一般
5、选择题 将磁性氧化铁放入稀HNO3中可发生如下反应:3Fe3O4+28HNO3=9Fe(NO3)x+NO↑+14H2O,下列判断合理的是
A.Fe(NO3)x中的x为2
B.磁性氧化铁中的铁元素全部被氧化
C.稀HNO3在反应中只作氧化剂
D.反应中每生成0.4 mol还原产物,就有1.2 mol电子转移
参考答案:D
本题解析:
试题分析:A、根据氮原子守恒可知28=9x+1,则x=3,A不正确;B、由于四氧化生铁还可以表示为FeO・Fe2O3,所以在反应中铁元素并没有全部被氧化,B不正确;C、根据方程式可知,反应中还有硝酸铁生成,所以硝酸好起到酸性的作用,C不正确;D、反应中氮元素的化合价从+5价降低到+2价,得到3个电子,即每生成1molNO转移3mol电子。NO是还原产物,所以反应中每生成0.4 mol还原产物,就有0.4mol×3=1.2 mol电子转移,D正确,答案选D。
考点:考查氧化还原反应的有关判断与计算以及硝酸性质的判断
本题难度:一般