微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在H2S的饱和溶液中存在下列平衡①H2S?H++HS-②HS-?H++S2-,且知K1>K2,采取下列哪种措施后,既可增大c(S2-)又能提高pH还能使电离平衡逆向移动的是( )
A.加NaOH
B.通入H2S气体
C.降温
D.加入Na2S晶体
参考答案:A.向溶液中加入氢氧化钠,氢氧化钠和氢离子反应生成水,则电离
本题解析:
本题难度:简单
2、选择题 常温下,现有0.01mol/L的下列溶液:①CH3COOH?②NaHCO3③NaHSO4④KOH?⑤H2SO4按pH由小到大的顺序排列的是( )
A.⑤③①②④
B.③⑤①②④
C.⑤②③①④
D.④②①③⑤
参考答案:A
本题解析:
本题难度:一般
3、选择题 下列说法正确的是
A.常温下物质的量浓度相等的①(NH4)2CO3 ②(NH4)2SO4③ (NH4)2Fe(SO4)2三种溶液中水的电离程度:③>②>①
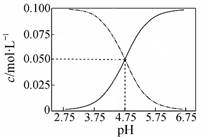
B.常温下醋酸和醋酸钠混合溶液中c(CH3COOH)、c(CH3COO-)与pH值的关系如图所示,当pH=4.5溶液中:c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-)
C.向Ca(OH)2溶液中加入过量的NaHCO3溶液:
Ca2++2HCO3-+2OH-→ CO32-+CaCO3↓+2H2O
D.25°C时,HCN溶液的电离平衡常数(Ka)与NaCN溶液的水解平衡常数(K)存在如下关系: Kw ・K = Ka
参考答案:D
本题解析:
试题分析:A、常温下物质的量浓度相等的①(NH4)2CO3?②(NH4)2SO4?③ (NH4)2Fe(SO4)2三种溶液中水的电离程度:①>③>②,错误;B、由题给图像可知,常温下pH=4.5的醋酸和醋酸钠混合溶液中c(CH3COOH)>c(CH3COO-),错误;C、向Ca(OH)2溶液中加入过量的NaHCO3溶液:Ca2++2HCO3-+2OH-→ CO32-+CaCO3↓+2H2O,正确;D、25°C时,HCN溶液的电离平衡常数Ka=[H+][CN―]/[HCN],NaCN溶液
本题难度:一般
4、选择题 醋酸溶液中存在电离平衡CH3COOH H++CH3COO-,下列叙述不正确的是(????)
H++CH3COO-,下列叙述不正确的是(????)
A.醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-)
B.0.10mol/L的CH3COOH溶液中加水稀释,溶液中c(OH-)减小
C.CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动
D.常温下pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7
参考答案:B
本题解析:
试题分析:A.在醋酸溶液中存在的阳离子是H+、阴离子是OH-和CH3COO-。根据电荷守恒可知,醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-)。正确。B.0.10mol/L的CH3COOH溶液中加水稀释,溶液中c(H+)减小。由于在溶液中存在Kw=c(H+)・c(OH-).所以c(OH-)增大。错误。C. 醋酸溶液中存在电离平衡CH3COOH 本题难度:一般
本题难度:一般
5、选择题 现有物质的量浓度均为0.1mol/L的下列5种物质的水溶液:①HNO3②H2SO4③CH3COOH??④NaOH其溶液中由水电离出的c(H+)的大小关系是( )
A.③>①=④>②
B.③=①=④>②
C.②>①>③>④
D.③>①>④>②
参考答案:A
本题解析:
本题难度:简单