微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 若NA表示阿伏加德罗常数,下列说法正确的是:
A.1mol H2O2含有极性共价键为NA,含有非极性键为2NA
B.2mol SO2和1mol O2在密闭容器中加热(V2O5催化)充分反应后,容器内分子总数为2NA
C.1molFeCl3完全转化为Fe(OH)3胶体后生成NA个胶粒
D.将0.1mol Cl2与足量NaOH溶液在常温下充分反应,转移的电子数为0.1NA
参考答案:D
本题解析:
试题分析:A、1mol H2O2含有极性共价键为2NA,含有非极性键为NA。B SO2和O2反应生成SO3是一个可逆反应,充分反应后该反应仍不能进行完全,故容器内的分子总数大于2NA。C选项1molFeCl3完全转化为Fe(OH)3胶体后生成胶粒个数小NA。D选项发生的反应为: Cl2+2NaOH=NaCl+NaClO+H2O, 该反应是一个歧化反应,既是氧化剂又是还原剂,所以Cl20.1mol Cl2与足量NaOH溶液在常温下充分反应,转移的电子数为0.1NA
点评:本题属于高考中的常见题
本题难度:一般
2、选择题 设NA为阿伏加德罗常数的值,下列关于2 L 0.2 mol・L-1的Ba(NO3)2溶液的说法不正确的是
①溶液中的阴、阳离子总数为0.8NA?②取0.5 L溶液则其中NO3-的浓度为0.1 mol・L-1
③取0.5 L溶液则其中Ba2+的浓度为0.2 mol・L-1 ④取0.5 L溶液则其中NO3-的总数为0.2NA
A.①②
B.③④
C.①④
D.②④
参考答案:B
本题解析:
试题分析:硝酸钡的物质的量为0.4mol,钡离子和硝酸根离子物质的量分别为0.4mol、0.8mol,阴、阳离子总数为1.2mol;硝酸钡溶液物质的量浓度为0.2mol/L,钡离子浓度为0.2mol/L,硝酸根离子物质的量浓度为0.4mol/L,取出0.5L溶液浓度不变;取出0.5L溶液中硝酸根离子物质的量为0.5L×0.4mol/L=0.2mol。
点评:浓度与体积无关。
本题难度:一般
3、填空题 某小组用铜屑制取硫酸铜溶液。将铜屑放入一定浓度的硫酸中,加热并不断鼓入空气其反应原理为2Cu+O2+2H2SO4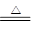 2CuSO4+2H2O。现欲将6.4 g铜完全溶解,加水后得200 mL溶液。计算:
2CuSO4+2H2O。现欲将6.4 g铜完全溶解,加水后得200 mL溶液。计算:
(1)参加反应的氧气在标准状况下的体积是 。
(2)所得硫酸铜溶液的物质的量浓度是 。
(3)取100 mL上述硫酸铜溶液,加水稀释至0.1 mol/L,稀释后硫酸铜溶液的体积是 。
参考答案:(1)1.12 L (2)0.5 mo
本题解析:
试题分析:(1)由方程式2Cu+O2+2H2SO4 2CuSO4+2H2O可知:n(Cu)=2n(O2). n(Cu)=6.4g÷64g/mol=0.1mol,所以n(O2)="1/2" n(Cu)=0.05mol,V(O2)= 0.05mol×22.4L/mol=1.12L.(2)n(CuSO4)= n(Cu)=0.1mol.C(CuSO4)="n/V=0.1mol÷0.2L=0.5" mol/L。(3)在溶液稀释前后溶质的物质的量不变。0.5 mol/L×0.1L="0.1" mol/LV,所以V="0.5" L="500" mL。
2CuSO4+2H2O可知:n(Cu)=2n(O2). n(Cu)=6.4g÷64g/mol=0.1mol,所以n(O2)="1/2" n(Cu)=0.05mol,V(O2)= 0.05mol×22.4L/mol=1.12L.(2)n(CuSO4)= n(Cu)=0.1mol.C(CuSO4)="n/V=0.1mol÷0.2L=0.5" mol/L。(3)在溶液稀释前后溶质的物质的量不变。0.5 mol/L×0.1L="0.1" mol/LV,所以V="0.5" L="500" mL。
考点:考查物质的量在气体的体积、物质的量浓度的溶液的计算及溶液稀释等计算的应用。
本题难度:一般
4、填空题 (8分)(1)两个同容积的密封容器A、B,常温下,A中充入a g A气体,B中充入a g CH4气体,A与B内的压强之比是4∶11,则A的摩尔质量为_________________。
(2)某氯化镁溶液的密度为d g/cm3,其中镁离子的质量分数为w,a mL该溶液中Cl-
的物质的量为 。
(3)标准状况下VL氨气溶解在1L水中(水的密度近似为1g/ mL),所得溶液的密度为ρ g/ mL, 则该溶液的溶质的物质的量浓度为 。
(4)在 11P + 15 CuSO4 +24 H2O =" 5" Cu3P +6 H3PO4 +15 H2SO4中,每 1 mol CuSO4可以氧化磷的物质的量是 __________ 。
参考答案:(每空2分,共8分)
(1)44 g/mol
本题解析:略
本题难度:一般
5、选择题 在标准状况下,气体A和B的密度分别为1.250 g・L-1,1.875 g・L-1,A、B的混合气体对H2的相对密度为16.8,则混合气体中A和B的体积比是(??? )
A.1∶1??????????? B.1∶2??????????????? C.2∶3??????????? D.3∶2
参考答案:D
本题解析:设A的物质的量是x,则n(B)为(1 mol-x)。
28x+42(1 mol-x)="33.6?" x="0.6" mol
n(A)="0.6" mol? n(B)="0.4" mol
n(A)∶n(B)=0.6∶0.4=3∶2。
本题难度:简单