��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ������ʾ��ͬŨ�ȵ�������п��Ӧʱ��������Ա���ԭΪSO2��Ҳ�ɱ���ԭΪ������Ϊ����֤��һ��ʵ��ijͬѧ������ͼװ�ý���ʵ�飨ʵ��ʱѹǿΪ10lkPa���¶�Ϊ0�棩��
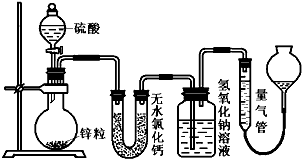
��1��������ƿ�з���1.30gп������c mol/L H2SO4��Ӧ��Ϊ��֤ʵ����۵Ŀɿ��������ܵ����˹����
__________��ѡ�200,400,500��mL��
��2����1.30gп����ȫ�ܽ⣬��������ϴ��ƿ����l.28g ����Բ����ƿ�з�����Ӧ�Ļ�ѧ����ʽΪ��
________________________��
��3������ƿ��Ͷ��agп����ȫ��Ӧ����������ϴ��ƿ����b g������ ƿ���ռ���Vm�����壬���У�
ag��65g��mol-1��bg��64g��mol-1��V mL / 22400 mL��mol-1�����ݵ�ԭ����____________________________��
��4��������ƿ��Ͷ��d gп������һ������c mol��L Ũ����V L����ַ�Ӧ��п��ʣ�࣬�����������ϴ��ƿ����mg��������ʵ����̲����������У�n��H2��/n��SO2����_______________���ú���ĸ�Ĵ���ʽ��ʾ����
��5�� ��Ӧ������Ϊ��ȷ�ز�������������������ڶ���ʱӦע�⣺___________________��
_________________��__________________��
�ο��𰸣���1��500
��2��Zn+2H2SO4(Ũ)==ZnSO4+SO2+2H2O
��3����ʧ�����غ�
��4��(64cV-2m)/m
��5����ȴ��ԭ�¶ȣ�©���к���������Һ����ƽ�������밼Һ�����ʹ���ˮƽ��
���������
�����Ѷȣ�����
2��ʵ���� ( 12�� ) ��ͼ��ʾ��װ�������Ʊ�1��2 -�������� ( ���ƿ�е�NaOH��Һ��Ϊ�����ո���Ӧ������SO2�� ) ����ش���������:
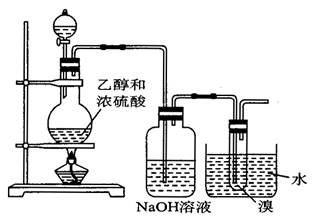
( 1 ) ���Ȼ������170 �� ������Ϊ�� ____________________ ��
( 2 ) ���ƿ��NaOH��Һ������д������SO2��Ӧ�Ļ�ѧ����ʽ ___________________ ��
( 3 ) ʹ��ˮ����ȴ����Ϊ��ʲô��
( 4 ) ��ƿ�еĻ��Һ����ʱ�ȱ���ɫ����ɫ������ _________________________ ��
( 5 ) ��ƿ�з�Щ�״�Ƭ����������ʲô��
( 6 ) ���ɵ�1��2 -��������ͨ�����й������壬Ϊϴȥ������� ______________ ��
�ο��𰸣�( 1 ) ����ϩ
? ( 2 ) SO2 + 2NaOH�T�TNa2SO3 + H2O
? ( 3 ) ��ֹ��ӷ�
? ( 4 ) ŨH2SO4ʹ�����Ҵ�����Ϊ̼
? ( 5 ) ��ֹ����
? ( 6 ) NaOH��Һ
��������������Ƕ�ʵ��������ϩ�Ŀ��飬ԭ����CH3CH2OH 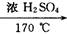 ?CH2�TCH2�� + H2O�����ڵĸ���Ӧ�Т�ŨH2SO4ʹ�Ҵ���ˮ̼����������2H2SO4 ( Ũ ) + C�T�T2SO2�� + CO2�� + 2H2O��Ӧ����CH3CH2OH + HO��CH2CH3
?CH2�TCH2�� + H2O�����ڵĸ���Ӧ�Т�ŨH2SO4ʹ�Ҵ���ˮ̼����������2H2SO4 ( Ũ ) + C�T�T2SO2�� + CO2�� + 2H2O��Ӧ����CH3CH2OH + HO��CH2CH3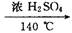 CH3CH2��O��CH2CH3 ( ���� ) + H2O�����Ա�������¶���170 ��,�����������ϩ���ʵ���֤��CH2�TCH2
CH3CH2��O��CH2CH3 ( ���� ) + H2O�����Ա�������¶���170 ��,�����������ϩ���ʵ���֤��CH2�TCH2 
�����Ѷȣ���
3������� ͼΪʵ������ȡ�����������Cl2�������м���Cl2����ʵ���װ�ã�����Eƿ�з��и����ɫ������F��Ϊͭ����F�Ҷ˳����ܿڸ���������֬�ޣ�
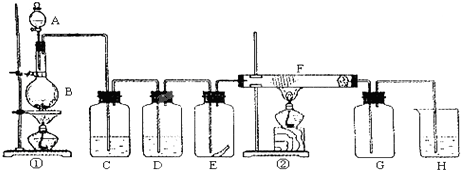
�Իش�
��1��A�Լ�Ϊ______��B�Լ�Ϊ______����ѧ����ʽΪ______��
��2��C�Լ�Ϊ______��D�Լ�����Ϊ______��
��3��E�и����ɫ����______�����ɫ������ɫ������
��4��F��������______��
��5��H�л�ѧ����ʽΪ______��
�ο��𰸣�������������������Ϣ��֪��ʵ��������ȡ�����������Cl2�������м���Cl2����ʵ�飮
��1�����ݿα���ѧ�Ʊ������õ���Ũ�������MnO2�ļ��ȷ�Ӧ������AΪŨ���ᣬBΪMnO2����Ӧ�Ļ�ѧ����ʽΪ��MnO2+4HCl-?��?.?MnCl2+Cl2��+2H2O��
�ʴ�Ϊ��Ũ���MnO2��MnO2+4HCl-?��?.?MnCl2+Cl2��+2H2O��
��2���ɢ�����������������ͨ��C�г�ȥ�ӷ�����HCl���壬��ȥHCl�����б���ʳ��ˮ�����CΪ����ʳ��ˮ��������C��ͨ�뵽D�н��и����ȥ������ˮ������D����Ũ���ᣬ
�ʴ�Ϊ������ʳ��ˮ����ˮ�����е�ˮ������
��3��������D�г������Ǹ����������ͨ��E�У��������������Ư�ף����E�еĸ��ﲼ������ɫ���ʴ�Ϊ������ɫ��
��4����֪F����ͭ�����ڼ��ȵ������£�������Cu������Ӧ�������ػ�ɫ���̣���֬��������Ϊ�˷�ֹ��ֹCuCl2����С������������뵼���У��������ܣ�Ӱ���������ռ���
�ʴ�Ϊ���ػ�ɫ���̣�
��5���������ж����壬����H�������ն��������NaOH��Һ����Ӧ�Ļ�ѧ����ʽΪCl2+2NaOH=NaCl+NaClO+H2O���ʴ�Ϊ��Cl2+2NaOH=NaCl+NaClO+H2O��
���������
�����Ѷȣ�һ��
4��ѡ���� ��4����Һ����ʵ�飬�±��С������������롰��Һ����Ӧ��ϵ��ȷ���ǣ�������
| ѡ�� | ���������� | ��Һ
A
ͨ��CO2����Һ����ǣ�����ͨ��CO2����������������ʧ��
����Na2CO3��Һ
B
ͨ��CO2����Һ����ǣ�����ͨCO2��������������ʧ��
Na2SiO3��Һ
C
ͨ��CO2����Һ����ǣ�����ͨ��CO2����������������ʧ���ټ���Ʒ����Һ����ɫ��ȥ��
Ca��ClO��2��Һ
D
ͨ��CO2����Һ����ǣ�����ͨCO2��������������ʧ���ټ�������NaOH��Һ���ֱ���ǣ�
Ca��OH��2��Һ
|
A��A
B��B
C��C
D��D
�ο��𰸣�A����Na2CO3��Һ��ͨ�������̼���ᷢ����Ӧ����̼�����ƣ�̼�����Ƶ��ܽ��С��̼���ƣ����Ի�����̼�����ƾ��壬��A��ȷ��
B����Na2SiO3��Һ��ͨ�������̼����������ᣬ�ǰ�ɫ������ˮ�ij���������ͨCO2�����������Dz�����ʧ����B����
C����Ca��ClO��2��Һ��ͨ�������̼��������̼��ƺʹ����ᣬ̼����ڹ���������̼�����»�ת��Ϊ̼����ƣ�������ʧ�����������ǿ�����ԣ���ʹƷ����ɫ����C����
D������������ͨ������̼������̼��Ƴ�������ת��Ϊ̼����ƣ�̼����ƺ��������Ʒ�Ӧ������̼��ƣ���D��ȷ��
��ѡAD��
���������
�����Ѷȣ���
5��ʵ���� ijѧУ��ѧ��ȤС��������Ԫ�����ڱ��е������ڵ�ijЩԪ��̽��Ԫ�صĽ����Ժͷǽ�������ԭ�������仯�Ĺ��ɡ�����ȤС��ѡ���ʵ���������Լ����ձ����Թܡ��ƾ��ơ�����ˮ��ϡ���ᡢ��̪��Һ�ȡ�
(1)��������ʵ���������Լ�������ȤС��Ҫ����ʵ��̽����Ԫ����____________��
(2)��̽������Ԫ�صĵ�����ˮ��Ӧʱ��Ϊ�˱�֤ʵ��İ�ȫ�ԣ�Ӧ����________����Թܡ����ձ������н��з�Ӧ��Ϊ����ʵ��֤����Σ�գ�������еIJ�����________________��
(3)��ˮ�е���1 mL��̪�Լ�����ʵ��ʱ������ʵ�������ֻ������ˮ��Ӧ����Һ�Ժ�ɫ��������λ ͬѧ�ó����ۣ��ơ�þ������ֻ��������ˮ��Ӧ��������������_________�����ȷ������ȷ�������������ȷ�����㻹����ˮ���֡��Լ��������ʵ��̽��þ�����Ľ�����ǿ�������ʵ�������__________________����Ԥ��ʵ������________________________��
(4)С���е�����һλͬѧ���ʵ��������̽����Щ�����Ľ����ԣ�����ʦɾ���˸�ͬѧ��Ƶ������Ʒ� Ӧ��ʵ�飬�������ʦ��������Ŀ����__________________����ͬѧ����֧�Թ��и�����2 mL ϡ���ᣬȻ��������һ֧�Թ��м���2ƬþƬ������һ֧�Թ��м���2Ƭ��Ƭ����Ӧ��ʼ��ʱ��������__________________��������ͬѧ����ʱ�ڵڶ�֧�Թ��м��������������ϴ�����������۲쵽���ŷ�Ӧ�Ľ��У�������ķ�ӦԽ��Խ�죬ֱ�����Ӧ�����ʷ���״̬�������Ʋ���������������������ԭ����_________________________��
(5)����С��ó�ʵ����ۣ�______________________��
�ο��𰸣�(1)�ơ�þ����
(2)�ձ������ձ��Ϸ�һ�鲣��Ƭ
(3)����ȷ������֧�Թ��зֱ����2 mL����ˮ���������зֱ����2~3�η�̪�Լ���Ȼ����һ֧�Թ��м���2ƬþƬ������һ֧�Թ��м���2Ƭ��Ƭ������þƾ��Ƽ��ȣ��۲��Թ�����Һ��ɫ�ı仯��þƬ����ˮ�������ݲ�����ˮ��Һ��Ϊdz��ɫ
(4)��Ϊ�����ᷴӦ�dz����ң���ֹ������ը�¹ʣ�þ�����ᷴӦ���ң������������ܹ���Ӧ���÷�Ӧ�Ƿ��ȷ�Ӧ�����ŷ�Ӧ�Ľ��У���ӦҺ���¶����ߣ���Ӧ���ʱ��
(5)����ԭ�������ĵ������ơ�þ�����Ľ�������������ͬ����Ԫ������Ԫ�������ĵ�����Ԫ�صĽ�������������ǽ���������ǿ��
���������
�����Ѷȣ�һ��